| Скачать .docx |
Реферат: Лабораторная работа: Кремнийорганические полимеры
Содержание
1. Кремнийорганические полимеры
1.1 Полиорганосилоксаны
1.2 Полиорганосилазаны
1.3 Полиэлементоорганосилоксаны
2. Получение полиорганосилоксанов с линейными цепями молекул (органосилоксановых эластомеров)
3. Получение полиорганосилоксанов с разветвленными и циклическими цепями
3.1 производство полидиметилфенилсилоксанов полиметилфенил-силоксанов и лаков на их основе
Задача 1
Задача 2
Список использованной литературы
1. Кремнийорганические полимеры
В настоящее время осуществлено промышленное производство кремнийорганических и кремнийэлементоорганических высокомолекулярных соединений трех классов — полиорганосилоксанов, поли-органосилазанов и полиэлементоорганосилоксанов.
1.1 Полиорганосилоксаны
Полиорганосилоксаны представляют собой полимеры, основная цепь которых состоит из чередующихся атомов кремния и кислорода с различными обрамляющими группами или органическими радикалами у атома кремния.
При получении полиорганосилоксанов протекает ряд процессов:
1) гидролиз или согидролиз (гидролитическая конденсация) орга-ногалогенсиланов или алкоксиорганосиланов;
2) ступенчатая поликонденсация продуктов гидролитической конденсации органогалогенсиланов или алкоксиорганосиланов;
3) каталитическая полимеризация или перегруппировка циклических продуктов гидролитической конденсации;
4) поликонденсация или полисоконденсация продуктов гидролитической конденсации с различными органическими соединениями.
Механизм процесса гидролитической конденсации органогалогенсиланов состоит в следующем.
При действии воды на алкил- или арилгалогенсиланы происходит гидролитические замещение атома галогена, находящегося у атома Si, гидроксильной группой и образование лабильных промежуточных продуктов — гидроксиор-ганосиланов.
Монофункциональные соединения типа R3 SiCl гидролизуются водой до триорганогидроксисиланов, которые легко конденсируются с образованием гексаорганодисилоксанов:
![]()
В зависимости от характера органического радикала и от условий реакции равновесие может быть сдвинуто в ту или иную сторону. Сами по себе гексаорганодисилоксаны не представляют большого практического интереса, поэтому и гидролиз монофункциональных триорганохлорсиланов имеет ограниченное значение. Использование же монофункциональных соединений для осуществления реакций совместного гидролиза и конденсации с ди- и трифункциональными алкил(арил)хлорсиланами позволяет получать полимеры с различной, заранее заданной длиной цепи в зависимости от мольных соотношений взятых компонентов, например:
![]()
При гидролизе и конденсации дифункциональных органогалогенсиланов типа R2 SiCl2 в зависимости от рН среды образуются линейные и циклические соединения:
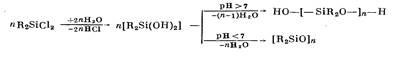
Органический радикал также оказывает значительное влияние на ход процесса. При гидролитической конденсации трифункциональных соединений в зависимости от условий реакции, применяемого растворителя и длины радикала, находящегося у атома Si, структура, состав и свойства полиорганосилоксанов, образующихся в результате гидролиза и поликонденсации, резко меняются, и это приводит к образованию полимеров с разветвленной I, сшитой или лестничной II структурой молекул:
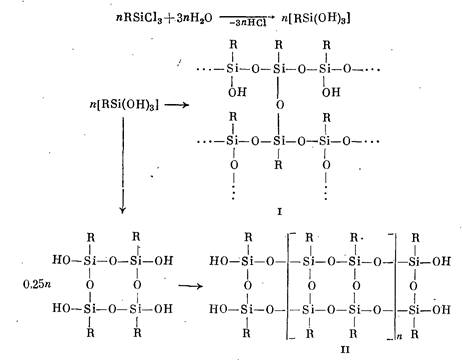
Полиорганосилоксаны в настоящее время выпускаются в виде:
1) олигомеров с линейными или циклическими цепями молекул (силиконовые жидкости);
2) полимеров с линейными цепями молекул (кремнийорганические эластомеры);
3) полимеров с циклолинейными, лестничными и разветвленными цепями молекул.
Общая схема технологического процесса производства полиорганосилоксанов:
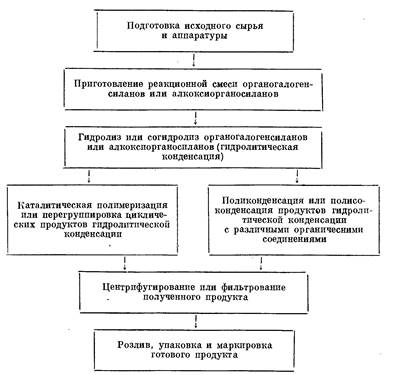
1.2 Полиорганосилазаны
Полиорганосилазаны представляют собой полимеры, основная цепь которых состоит из чередующихся атомов кремния и азота с различными обрамляющими группами или органическими радикалами у атома кремния. Для синтеза полиорганосилазанов можно осуществлять реакцию аммонолиза или соаммонолиза органогалогенсиланов с последующей конденсацией или полимеризацией образующихся продуктов. Например, аммонолизом диорганодихлорсиланов образуются диорганоциклосилазаны.
![]()
При анионной полимеризации диорганоциклосилазанов получаются органосилазаны полициклического строения (в отличие от полимеризации органосилоксанов):

Полиорганосилазаны выпускаются в виде олигомеров циклического или линейного строения и полимеров с разветвленными и циклолинейными цепями молекул.
1.3 Полиэлементоорганосилоксаны
Полиэлементоорганосилоксаны представляют собой полимеры, основная цепь которых состоит из чередующихся атомов кремния, кислорода и другого элемента (например, алюминия или титана) с различными обрамляющими группами или органическими ради-, калами у атома кремния. Получение полизлементоорганосилоксанов может быть осуществлено либо реакцией обменного разложения полиорганосиланолятов щелочных металлов солями металлов, либо путем гетерофункциональной конденсации а,со-дигидроксидиорга-носилокеанов с алкоксипроизводными металлов. Молекулы полиэлементоорганосилоксанов имеют разветвленную, лестничную или циклолинейную структуру.
2. Получение полиорганосилоксанов с линейными цепями молекул (органосилоксановых эластомеров)
Полиорганосилоксаны с линейными цепями молекул
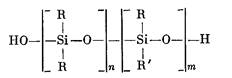
где 1) R и R' — метил; 2) R — метил, aR' — винил; 3) R — метил, aR' — фенил и др., получают реакциями гидролитической поликонденсации или полисоконденсации дифункциональных органохлор-силанов.
Дифункциональные органохлорсиланы при гидролизе проявляют большую склонность к циклизации. Так, например, диметилдихлорсилан гидролизуется водой (в отсутствие растворителя) по конденсационно-полимеризационному механизму с образованием смеси диметилсилоксанов линейного и циклического строения:
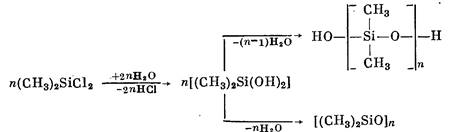
Образование циклических соединений возрастает с величиной органических.радикалов, связанных с кремнием. Например, метил-фенилдихлорсилан и дифенилдихлорсилан образуют при гидролизе преимущественно циклические продукты. В процессе образования циклов при гидролизе органодихлорсиланов важную роль играют условия реакции, в частности рН среды. С увеличением рН, т. е. с уменьшением кислотности среды, можно уменьшить процесс образования циклов, но полностью избежать его невозможно.
Поэтому при получении полидиорганосилоксанов с линейными цепями молекул важнейшей реакцией является полимеризация циклов, образующих-ся при гидролитической поликонденсации диорганодихлорсиланов. Для раскрытия молекул органоциклосилоксанов и получения линейных полиоргано-силоксанов используют реакцию каталитической полимеризации. В качестве инициаторов полимеризации применяются инициаторы катионного типа H2 S04 , Н3 В03 , Н3 Р04 , НООС—СООН, BF3 и др. и анионного типа, например NaOH, КОН, R3 SiONa, и др.
При катионной полимеризации, например, с серной кислотой процесс заключается в следующем: на начальной стадии инициирования при взаимодействии органоциклосилоксана с серной кислотой протон кислоты атакует атом кислорода силоксанового цикла. В результате перераспределения электронной плотности связь Si—О разрывается с раскрытием цикла и образованием активного центра на конце цепи:
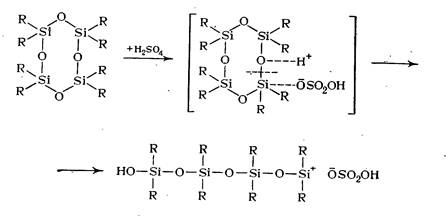
Образовавшийся активный центр ведет дальнейший процесс полимеризации (рост цепи), сопровождающийся размыканием следующих циклов:
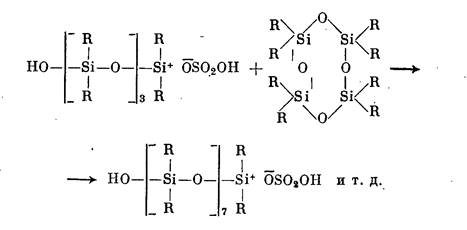
Превращение циклов в линейную полимерную цепь продолжается до достижения равновесия в системе. Обрыв цепи связан с переносом заряда при взаимодействии макрокатиона с молекулами серной кислоты или с захватом макрокатионом присутствующих в системе анионов:
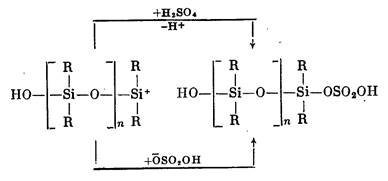
В случае полимеризации органоциклосилоксанов в присутствии анионных инициаторов, например сс-окси-ю-тетраметиламмоний-оксидиметил силок сана, анион взаимодействует с атомом кремния. При этом происходит координационное связывание нуклеофильного реагента с циклом, ослабление кремний-кислородной связи и раскрытие цикла:
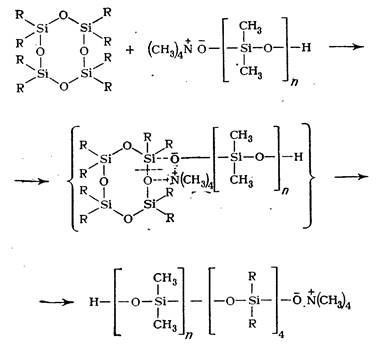
Образующийся активный центр взаимодействует далее со следующей циклической молекулой, раскрывая ее:
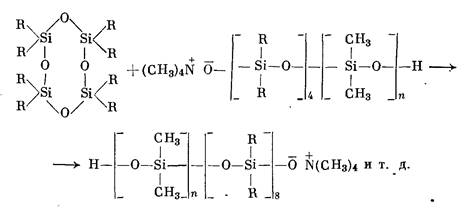
Превращение циклов в линейную полимерную цепь происходит и в этом случае в результате взаимодействия активного центра со следующими циклическими молекулами и тоже продолжается до достижения равновесия.
Обрыв цепи в обоих случаях каталитической полимеризации происходит при потере активности, т. е. при потере концевыми группами способности присоединять циклические молекулы. Это может быть следствием отщепления концевых групп — путем омыления сульфатных групп водой (в случае катионной полимеризации) или путем термической деструкции тетраметиламмониевых групп (в случае анионной полимеризации).
В настоящее время выпускается несколько марок органосилоксановых эластомеров: полидиметилсилоксан (СКТ), полидиметилметилвинилсилокса-ны (СКТВ и СКТВ-1, различающиеся содержанием метилвинил-силоксизвеньев), полидиметилдиэтилсил-оксан (СКТЭ), полидиметилме-тилфенилсилоксан (СКТФ), низкомолекулярные полидиметилсилоксаны (СКТН и СКТН-1, различающиеся молекулярным весом), полиметилфе-нилсилоксан (СКТМФ) и др.
3. Получение полиорганосилоксанов с разветвленными и циклическими цепями
Полиорганосилоксаны разветвленного I и лестничного II строения получают гидролитической поликонденсацией трифункциональных кремнийорганических соединений (лестничные полимеры) или смеси ди- и трифункциональных соединений (разветвленные полимеры).
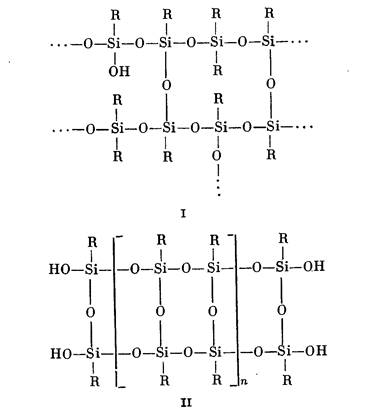
Решающее влияние на свойства полиорганосилоксанов разветвленного и лестничного строения оказывают два фактора: функциональность исходных мономеров, определяемая соотношением числа органических групп или радикалов в них к атому кремния и степень использования функциональных групп в процессе синтеза полимеров. Когда соотношение R : Si снижается с 2 до 1, полимеры постепенно делаются менее текучими, плавкими и растворимыми — в зависимости от эффективности сшивания. При R:Si = 1, т. е. когда в качестве исходного сырья применяются лишь трифункцио-нальные мономеры (метилтрихлорсилан, фенилтрихлорсилан или смесь метил- и фенилтрихлорсиланов), образуются жесткие полимеры, а это значит, что их растворы в органических веществах (лаки) образуют при отверждении трехмерную жесткую структуру. При полном использовании функциональных групп получаются в основном неплавкие и нерастворимые сшитые продукты; однако при том же самом соотношении R : Si специальные методы обработки исходных органотрихлорсиланов могут приводить к лестничным структурам молекул с образованием гибких высокоплавких или неплавких, но растворимых продуктов.
Введение в основную цепь полимера дифункциональных звеньев (диметилсилокси-, диэтилсилокси- или метилфенилсилоксизвеньев) приводит к образованию эластичных полимеров циклолинейной структуры:
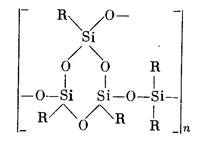
Таким образом, с увеличением соотношения R : Si и уменьшением числа сшивок можно получить полимеры от стеклообразных до каучукоподобных. Большинство полимеров циклолинейного и разветвленного строения получается при соотношении R : Si в пределах 1,0—1,6.
Большое влияние на свойства полиорганосилоксанов оказывает и природа органических групп R, обрамляющих атомы кремния. Увеличение длины алкильных радикалов делает полимер более мягким, повышает его растворимость в органических растворителях и гидрофобизирующую способность, но уменьшает стойкость к термоокислительной деструкции и нагреванию; фенильные радикалы повышают термостойкость полимера. Широкое распространение получили полиорганосилоксаны, содержащие фенильные и метальные группы в обрамлении главной цепи молекулы.
Наряду с такими положительными свойствами полиорганосилоксанов, как высокие тепло- и морозостойкость, хорошая гидрофобность и повышенные диэлектрические характеристики, они обладают недостаточно высокими физико-механическими показателями. Для улучшения этих качеств их часто модифицируют различными органическими полимерами (полиэфирными, эпоксидными и др.).
В настоящее время промышленность выпускает большой ассортимент полиорганосилоксанов разветвленного, циклолинейного и лестничного строения, различающихся по типу органических групп или радикалов, стоящих у атома кремния. Процесс производства таких полиорганосилоксанов основан на реакциях гидролиза или согидролиза органохлорсиланов и последующей поликонденсации продуктов согидролиза.
Основные классы полиорганосилоксанов разветвленного, циклолинейного и лестничного строения такие:
1) полиметилсилоксаны;
2) полифенилсилоксаны;
3) полидиметилфенилсилоксаны и полиметилфенилсилоксаны;
4) полидиэтилфенилсилоксаны;
5) полиалкилсилоксаны с алкильными радикалами С4 и более у атома Si.
кремнийорганический полиорганосилоксан молекула согидролиз
3.1 производство полидиметилфенилсилоксанов полиметилфенил-силоксанов и лаков на их основе
Полидиметилфенилсилоксаны получают согидролизом ди- и три-функциональных органохлорсиланов и последующей поликонденсацией полученных продуктов.
При согидролизе ди- и трифункциональных органохлорсиланов в кислой среде создаются благоприятные условия для взаимодействия (по схеме межмолекулярной конденсации) циклических соединений I образовавшихся в результате внутримолекулярной дегидратации алкил- и арилтригидроксисиланов, с продуктами гидролиза диоргано-дихлорсиланов, имеющими линейную структуру.
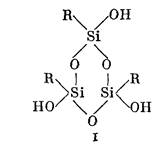
В результате при дальнейшей поликонденсации продуктов согидролиза образуются циклолинейные полимеры строения II:
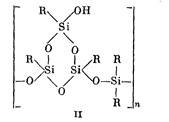
Полимеры подобного строения являются эластичными веществами, а при получении полиметилфенилсилоксанов согидролизом только трифункциональных мономеров (например, метил- и фенилтрихлорсиланов) образуются полимеры с малой эластичностью. Полидиметил- и полиметилфенилсилоксаны можно модифицировать различными органическими полимерами (полиэфирными, эпоксидными) или кремнийорганическими веществами (например, метилфениламиноме-тилдиэтоксисиланом). При модифицировании полидиметил- и полиметилфенилсилоксанов улучшаются многие свойства этих полимеров и лаков на их основе, в частности значительно повышаются адгезия и механическая прочность лаковых пленок.
Производство полидиметил- и полиметилфенилсилоксанов и лаков на их основе состоит из двух основных стадий: согидролиза органохлорсиланов; отгонки растворителя и приготовления лака.
Исходное сырье: метилтрихлорсилан (т. кип. 65—67 °С; 69,8— 71,2% Хлора), диметилдихлорсилан (фракция 67—70,3 °С; не более 56,5% хлора) или метилфенилдихлорсилан (фракция 196—204 °С; 36,9—37,8% хлора), фенилтрихлорсилан (фракция 196—202 °С; 49-50,5% хлора), толуол (т. кип. 109-111 °С; df= 0,865±0,003), бутиловый спирт (т. кип. 115—118 °С), полиэфир — продукт поликонденсации этиленгликоля с фталевым и малеиновым ангидридами.
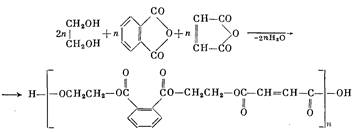
Модифицированный касторовым маслом (вязкость по ВЗ-4 при 20 °С не более 20 сек) или эпоксидный полимер — продукт взаимодействия эпихлоргидрина с дифенилолпропаном содержащий не более 21% эпоксигрупп, и метилфениламинометил-диэтоксисилан (т. кип. 110—120 °С при 1—2 мм рт. ст.).
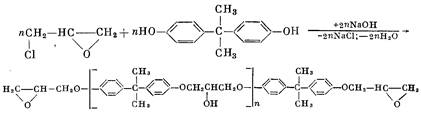
Принципиальная технологическая схема периодического процесса производства полидиметилфенилсилоксановых и полиметилфенил-силоксановых лаков приведена на рис. 82. В смеситель 6 из мерников 1, 2, 3 ж 4 через весовой мерник 5 загружают соответственно толуол и органохлорсиланы (метилтрихлорсилан, диметилдихлор-силан или метилфенилдихлорсилан и фенилтрихлорсилан) согласно рецептуре лака. По окончании загрузки смесь перемешивают в течение 1—2 ч — до удовлетворительного анализа на содержание хлора. Готовую смесь передавливают в мерник-дозатор 7 и направляют на согидролиз в эмалированный аппарат 10 с мешалкой и пароводяной рубашкой. Перед началом синтеза проверяют состояние эмали в аппарате и замазывают поврежденные места диабазовой замазкой.
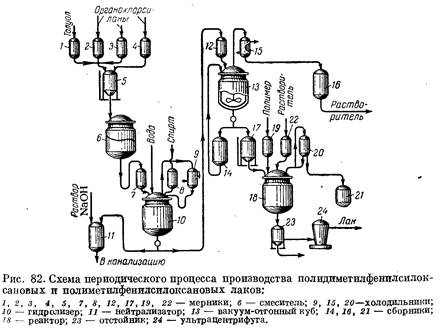
Согидролиз, как правило, проводится в избытке воды. В гидро-лизер подают воду, а затем вводят соответствующее количество бутилового или этилового спирта (в зависимости от марки лака). После этого из мерника-дозатора 7 по сифону в гидролизер при работающей мешалке вводят реакционную смесь с такой скоростью, чтобы температура в аппарате не повышалась сверх 30—50 °С.
После ввода всей реакционной смеси перемешивают смесь еще 30 мин, затем останавливают мешалку и отстаивают смесь 1—1,5 ч. После отстаивания определяют кислотность нижнего слоя и сливают его в нейтрализатор 11, а верхний слой (раствор продукта согидролиза в толуоле) промывают водой до нейтральной реакции.
Готовым продуктом на этой стадии является раствор гидроли-зата с содержанием смолы 25—30%. Его подают в мерник 12 и затем в вакуум-отгонный куб 13. Продукт там нагревают до 80—90 °С и после отстаивания сливают воду. Промежуточный слой сливают в сборник 14, откуда он снова поступает в отгонный куб. Затем в кубе создают остаточное давление 150—400 мм рт. ст. и поднимают температуру до 100—120 °С. При этом режиме и отгоняется растворитель.
Растворитель поступает в сборник 16 и оттуда на регенерацию толуола, а гидролиэат (концентрация полимера 45—50%) выгружают в весовой мерник 17, откуда он поступает на конденсацию в реактор 18. В случае производства модифицированных лаков в реактор загружают также полиэфир или эпоксидный полимер из мерника 19. Смесь в реакторе перемешивают 1 ч и после этого начинают отгонять растворитель при остаточном давлении 150— 300 мм рт. ст. Растворитель отгоняется со скоростью 40—60 л/ч до достижения температуры 120 °С. При этой температуре отгонку прекращают, прямой холодильник 20 включают как обратный, поднимают температуру до 130—160 °С (при остаточном давлении 200—500 мм рт. ст.) и начинают конденсацию.
В процессе конденсации из реактора 18 отбирают пробу для определения времени желатинизации полимера при 200 или 250 °С (в зависимости от марки лака). Конденсацию считают законченной при времени желатинизации 0,5—7 мин.
После завершения процесса конденсации прекращают подачу пара в рубашку реактора 18 и доводят в нем давление до атмосферного. В рубашку аппарата дают воду и из мерника 22 вводят необходимое количество растворителя для приготовления лака (50— 65%-ной концентрации). Включают мешалку и перемешивают лак 2—3 ч. После этого продукт анализируют и сливают лак в отстойник 23. Там лак отстаивается при температуре окружающей среды в течение 24 ч (или дольше) и затем самотеком поступает на ультрацентрифугу 24. В процессе центрифугирования через каждые 30 мин отбирают пробу для контроля внешнего вида лака. Готовый лак направляют на расфасовку. Описанный периодический способ имеет, однако, существенные недостатки:
1) небольшая мощность оборудования;
2) низкая производительность труда;
3) многостадийность процесса, поэтому приходится многократно перегружать полупродукты и готовый лак из аппарата в аппарат, что зачастую приводит к нарушениям технологического процесса, к браку продукции и загазованности на рабочем месте;
4) затруднена автоматизация процесса;
5) высокая себестоимость полимеров и лаков на их основе.
Этих недостатков лишен непрерывный процесс производства полидиметилфенилсилоксановых и полиметилфенилсилоксановых лаков, принципиальная схема которого приведена на рис. 83.
Раствор смеси органохлорсиланов в толуоле из мерника-дозатора 1 поступает в струйный смеситель 3; сюда же подается в заданном соотношении вода. Расход компонентов контролируется ротаметрами. Реакция согидролиза происходит в камере смешения смесителя 3. Для завершения согидролиза реакционную смесь направляют в колонну 4, из которой массу сливают в флорентийский сосуд 5. В этом сосуде продукты согидролиза и соляная кислота расслаиваются.
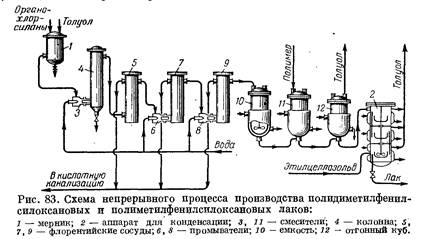
Кислоту сливают в канализацию, а гидролизат подвергают двухступенчатой промывке водой в промывателях 6 л 8, по конструкции аналогичных струйному смесителю. Гидролизат промывают до рН 5—6 и отделяют от промывных вод в флорентийских сосудах 7 и 9 и в емкости 10.
Из емкости 10 промытый гидролизат поступает для частичной отгонки растворителя в куб 12; в случае получения модифицированных полиметилфенилсилоксановых лаков гидролизат сначала смешивают с полиэфиром или эпоксидным полимером в аппарате 11, а затем направляют в куб. Из куба гидролизат направляется на конденсацию в трехсекционнып аппарат 2. В первой секции осуществляется дополнительная отгонка растворителя и частичная конденсация продукта согидролиза, во второй — дальнейшая конденсация при 125—180 °С (в зависимости от марки лака), в третьей — растворение конденсированного полимера для приготовления лака нужной концентрации (растворитель — этилцеллозольв).
Аппарат 2 колонного типа разделен внутренними поперечными перегородками на три секции. Каждая секция имеет якорную мешалку, закрепленную на общем валу, и паровую рубашку. Жидкость из одной секции в другую переливается по внутренним трубкам. Такая конструкция позволяет проводить непрерывный процесс конденсации, не опасаясь внезапного гелеобразования. Все основные аппараты в схеме непрерывного производства лаков расположены каскадом, благодаря чему обеспечивается полный самотек основного продукта по всей технологической нитке
Сравнивая непрерывный процесс производства лаков с периодическим, можно отметить следующие преимущества непрерывного процесса:
1) мощность оборудования возрастает более чем в 10 раз;;
2) в 10 раз возрастает производительность труда;
3) за счет снижения потерь сырья и полупродуктов значительно уменьшаются расходные коэффициенты;
4) непрерывный процесс легко управляем, поэтому его можно полностью автоматизировать.
Все эти преимущества позволяют в полтора-два раза снизить себестоимость лаков при непрерывном процессе производства.
Полидиметилфенилсилоксановые и полиметилфенилсилоксановые лаки представляют собой прозрачные жидкости от светло-желтого до светло-коричневого цвета. Они растворимы в толуоле, бензоле, ксилоле и других неполярных органических растворителях, но нерастворимы в воде и спиртах.
Свойства этих лаков зависят прежде всего от исходных мономеров. Как отмечалось выше, в производстве лаков используются как нефункциональные мономеры (например, диметил- или метил-фенилдихлорсилан), так и трифункциональные (метилтрихлорсилан, фенилтрихлорсилан и др.). Увеличение содержания дифункциональ-ного мономера в смеси органохлорсиланов обеспечивает большую эластичность лаковой пленки, но при этом снижаются ее твердость п время перехода лака в неплавкое и нерастворимое состояние. Увеличение количества трифункционального мономера (фенилтри-хлорсилана) в смеси повышает термостойкость и блеск пленки, но при этом время перехода лака в неплавкое и нерастворимое состояние значительно увеличивается по сравнению с лаками, содержащими метилсилсесквиоксановые звенья.
Полидиметилфенилсилоксановые и полиметилфенилсилоксановые лаки широко применяются в электротехнической промышленности. Некоторые из них (например, лаки на основе метил- и фенил-трихлорсиланов) в определенных условиях могут быть использованы в качестве связующих для прессматериалов, однако обычно для перевода этих лаков в неплавкое и нерастворимое состояние требуется длительное нагревание, и поэтому для получения слоистых пластиков они практически непригодны.
Задача 1
В каскад автоклавных реакторов полимеризации этилена при среднем давлении подают 8000 м3 этилена в час. В качестве растворителя используют бензин. На снятие выделяющейся теплоты расходуют 90 % этилена и 35% бензина. Определить массовый расход бензина, если массовая доля полиэтилена в растворе, выходящем из каскада реакторов, равна 20%.
Дано: VЭ = 8000 м3 На снятие теплоты Э – 90% Бенз. – 35%
|
Решение: п СН2 =СН2 [– СН2 – СН2 –] п 1) Массовый расход этилена, поданного в реактор 2) Расход этилена, поданного на снятие выделяющейся теплоты 3) Масса ПЭ 4) Масса раствора, выходящего из реактора 5) Массовый расход бензина Ответ: 6154 кг/ч |
Задача 2
Производительность установки полимеризации винилацетата равна 400 кг полимера в час. Массовое соотношение винилацетата и метанола на входе в полимеризатор 23:1; массовая доля полимера в метаноле, отбираемого из двух последовательных реакторов колонного типа объемом 5 и 12 м3 , равна 20%. Полимеризацию ведут до 70% степени конверсии мономера. Определить коэффициенты заполнения реакторов, если время пребывания реакционной массы в каждом аппарате равно 4 часа. Плотность реакционной массы в первом реакторе 950 кг/м3 , во втором – 820 кг/м3 .
Дано: G= 400 кг/ч ВА : метанол 23 : 1
V1 – 5 м3 V2 – 12 м3
τ – 4 ч К1 , К2 – ? |
Решение: п СН2 =СН [– СН2 – СН –] п СН3 С - О СН3 С - О О О 1) Масса раствора на выходе из второго реактора 2) Объем реакционной массы второго реактора 3) Коэффициент заполнения второго реактора 4) Масса мономера, поступающего в первый реактор 5) Масса метанола, поступающего в первый реактор 6) Объем реакционной массы первого реактора 7) Коэффициент заполнения первого реактора Ответ: 0,5 и 0,81 |
Список литературы
1. Грандберг И.И. Органическая химия. – М.: Высшая школа, 1980. – 463 с.
2. Перекалин В.В. и др. Органическая химия. – М.: Просвещение, 1982. – 543 с.
3. Третьяков Ю.Д. Химия: Справочные материалы. – М.: Просвещение, 1984. – 239 с.
4. Фурмер И.Э. Общая химическая технология. – М.: Высшая школа, 1987. – 334 с.
5. Хомченко Г.П. Химия для поступающих в ВУЗы. – Высшая школа, 1985. – 357 с.
6. Хананашвили Л.М. Технология элементоорганических мономеров и полимеров. – М. : Химия, 1973. – 400 с.