| Скачать .docx |
Реферат: Назначение процесса сернокислотного алкилирования изопарафинов олефинами. Пиролиз
Назначение процесса сернокислотного алкилирования изопарафинов олефинами. Основные и побочные реакции, приведите механизм. Условия проведения процесса. Технологические особенности процесса и связанные с ними технические решения, какими стадиями представлен процесс. Выбор типа и конструкции реактора
Этот процесс предназначен для синтеза высокооктановых компонентов авиационных и автомобильных бензинов. Для случая алкилирования изобутана изобутиленом реакция может быть представлена в следующем виде:
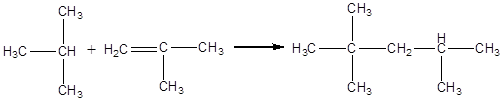
Реакция сернокислотного алкилирования изопарафинов олефинами протекает избирательно. Легче всего подвергаются алкилированию изобутан и изопентан, т.е. изопарафиновые углеводороды, содержащие один третичный атом углерода в молекуле. Парафиновые углеводороды с четвертичным атомом углерода в молекуле типа 2,2-диметилбутана алкилируются значительно труднее и при более жестких условиях. Парафины нормального или изостроения, содержащие в одновременно с третичным четвертичный атом углерода, в присутствии серной кислоты практически не алкилируются.
Олефины для алкилирования могут быть взяты различные. Однако этилен наименее эффективный алкилирующий агент. Алкилирование пропиленом и н-бутенами дает хорошие результаты, при алкилировании изоамиленами начинают в большом количестве образовываться продукты деструктивного алкилирования, а при алкилировании высшими олефинами эти реакции начинают преобладать.
Как правило, алкилируют изобутан н-бутенами, т.к. при этом образуются изомерные углеводороды C8H18 (триметилпентаны), по температуре кипения наиболее пригодные в качестве компонента моторных топлив. Углеводороды C8H18, но другого вида (диметилгексаны) получаются и при алкилировании изопентана пропиленом, кроме того, изопентан является ценным сырьем для получения изопрена, поэтому для алкилирования его используют редко (иногда добавляют к изобутану).
Строение продуктов, образующихся при каталитическом алкилировании изопарафинов олефинами, обычно не соответствует ожидаемому из структуры исходных веществ. При взаимодействии н-бутенов с изобутаном получается смесь 2,2,4-, 2,3,4- и 2,3,3-триметилпентаны.
Причина несоответствия строения продуктов состоит в особенностях механизма реакции, осложненной процессами изомеризации. Механизм алкилирования цепной карбоний-ионный:
небольшие порции олефина (бутен-2) взаимодействуют с протоном кислоты;
возникающий вторичный карбокатион, образовавшийся из н-бутена, менее стабилен, чем третичный, вследствие чего происходит быстрый обмен гидрид-иона с изобутаном;
образующийся трет-бутилкатион взаимодействует далее с исходным олефином, с образованием карбокатиона большего молекулярного веса;
получившийся карбокатион склонен к внутримолекулярным перегруппировкам, сопровождающимся миграцией водорода и метильных групп;
эти карбокатионы взаимодействуют с изобутаном, в результате чего получаются углеводород C8H18 и третбутилкатион, обеспечивающий протекание ионно-цепного процесса
Побочные реакции:
1. в условиях реакции алкилирования часть карбокатионов, образовавшихся из изопарафинов в присутствии катализатора теряет протон и образует соответствующий олефин, который взаимодействует с новым карбокатионом по обычной схеме и образует предельный углеводород, т.е. происходит автоалкилирование изопарафинов.
2. В случае недостатка олефина автоалкилирование приводит к избыточному расходу изопарафина.
3. Изооктилкатион также способен к реакции с олефинами. Так происходят последовательно-параллельные реакции алкилирования, причем, чтобы подавить образование высших углеводородов, необходим избыток изопарафина по отношению к олефину.
4. Реакция автоалкилирования осложняется, кроме того, деструкцией части образующихся углеводородов, в результате чего получаются более низкомолекулярные продукты. Этой реакции способствует повышение температуры.
5. Еще одна побочная реакция – это катионная полимеризация олефина, при которой получаются низкомолекулярные ненасыщенные полимеры, несколько ухудшающие качество алкилата и ведущие к повышенному расходу катализатора.
6. Часть олефинов взаимодействует с концентрированной серной кислотой с выделением двух молекул воды.
Обоснование условий сернокислотного алкилирования изобутана бутенами:
Реакция алкилирования изопарафинов олефинами экзотермична. При температуре ниже 1000С равновесие смещается вправо, реакция становится практически необратимой. Температуру алкилирования выбирают такой, чтобы максимально подавлялись побочные реакции деструкции и полимеризации, но сохранялась достаточно высокой скорость процесса. В данном случае температура поддерживается 5-130С.
Давление не оказывает существенного влияния на этот низкотемпературный жидкофазный процесс. Его выбирают по технологическим соображениям несколько большим, чем давление перерабатываемых углеводородов при температуре в реакторе, чтобы обеспечить поддержание их в жидкой фазе. При снятии тепла реакции за счет испарения части углеводородов увеличение давления нецелесообразно, т.к. затрудняет испарение. При алкилировании изобутана бутенами поддерживают давление 0,35-0,4 МПа.
Концентрация кислоты должна быть не менее 88-86%. в процессе работы она разбавляется высокомолекулярными соединениями (эфиры серной кислоты, ВМ углеводороды) и водой, приходящей с сырьем и выделяющейся в результате некоторых побочных реакций. Поэтому кислоту приходится укреплять.
Соотношение кислота : углеводороды поддерживают от 1 : 1 до 2 : 1.
Соотношение изобутан : олефин берут от 4 : 1 до 10 : 1. Чем выше концентрация изобутана в сырье, тем более благоприятны условия для протекания основной реакции алкилирования и подавления полимеризации и других побочных реакций.
Технологические особенности процесса:
необходимость создания стойкой эмульсии кислота - углеводороды – необходимо интенсивное перемешивание;
реакция идет при низких температурах и экзотермична – необходим интенсивный отвод тепла и поддержание изотермического режима;
использование большого избытка изобутана приводит к большой кратности циркуляции реакционной массы и необходимости отделять и возвращать непрореагировавший изобутан;
в процессе происходит разбавление серной кислоты – необходимо отводить часть ее на укрепление и добавлять свежую.
необходимо отстаивать серную кислоту и отмывать ее остатки из реакционной массы.
Стадии, из которых состоит процесс сернокислотного алкилирования:
подготовка сырья – очистка углеводородных потоков от примесей (сероводород, меркаптаны, вода) – щелочная и водная промывки, осушка от воды с помощью адсорбентов.
реакторное отделение;
обработка углеводородной смеси, выходящей из реакторов – отстаивание от кислоты, нейтрализация остатков кислоты щелочью, горячая водная промывка
фракционирование продуктов – сначала в первой колонне отделяются изобутан и пропан от остальных продуктов, затем пропан отделяется от изобутана, далее н-бутан отделяют от алкилата.
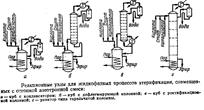
Для алкилирования применяются реакторы разных типов:
емкостные с применением выносных циркуляционных насосов для перемешивания реакционной смеси (в нижней части расположены тарелки или перегородки для интенсивного смешения компонентов);
контакторные с внутренними циркуляционными устройствами и охлаждающими элементами (вертикальные и горизонтальные – отличительная особенность последних – охлаждение с помощью потока продуктов, отходящих из реактора, а также инжекционный ввод сырья и кислоты);
каскадные с внутренним охлаждением и внутренними циркуляционными устройствами без охлаждающих элементов (горизонтальный аппарат, разделенный перегородками на реакционную и отстойную зоны)
В зависимости от системы охлаждения применяемые реакторы также делятся на три типа:
с замкнутым холодильным циклом и использованием хладагентов – аммиака, пропана, бутана (емкостные и контакторные реакторы);
с охлаждением отходящим потоком за счет его испарения при снижении давления в аппаратах, следующих за реактором, и дальнейшей конденсацией паров потока перед возвращением в реактор (контакторные реакторы);
с внутренним охлаждением путем испарения содержащихся в реакционной смеси пропана и изобутана при пониженном давлении внутри реактора (каскадные реакторы).
Пиролиз. Назначение процесса. Напишите механизм пиролиза на примере пентана. Ряд по возрастанию устойчивости соединений при пиролизе от метана до пентана, включая изомеры и непредельные соединения. Технологические приемы при пиролизе для увеличения выходов продукта.
Пиролиз - процесс получения низших олефинов.

Метан – Этилен – Этан – Пропан - Пропилен – Первичный - Вторичный - Третичный
Увеличение выхода обеспечивают паром или еще лучше водородом
Риформинг. Назначение процесса. Катализаторы риформинга. Какие возможны реакторные схемы риформинга. Объясните принцип их работы. Как изменяется температура в ходе процесса в зависимости от времени работы катализатора и от технологической схемы. Приведите уравнения протекающих реакций.
Основным назначение kt риформинга до настоящего времени остается повышение детонационной стойкости моторных топлив, однако не меньшее значение имеет и применение этого процесса для получения ароматических у/в – бензола, толуола и ксилолов.
В качестве катализаторов используют бифункциональные катализаторы, представляющие собой металлы платиновой группы, нанесенные на окись алюминия и промотированные галогеном. Катализаторы бывают монметалическими (платина на оксиде алюминия) и полиметалическими.
Полиметаллические kt риформинга наряду с Pt содержат несколько других металлов. Используемые для промотирования металлы можно разделить на 2 группы. К первой из них относятся иридий, рений, хорошо известные как kt гидро- и дегидрогенизации и гидрогенализа. Другая, более обширная группа промоторов, включает металлы, которые практически не активны в указанных реакциях. Такими металлами являются медь, кадмий, германий, олово, свинец и др. Большей частью также системы содержат, наряду с платиной, еще два элемента, из которых один принадлежит к первой группе, а другой – ко второй. Так, если Al – Ptkt промотируют репием, то в kt вводят еще один из следующих металлов: Cu, Ag, кадмий, цинк, индий, редкоземельные элементы – лантан, церий, неодим и др.
В качестве кислотного промотора в полиметаллических kt используется только хлор, массовое содержание его в kt 0,8-1,1%.
Технологически процесс осуществляется с неподвижным или движущимся слоем катализатора. При неподвижном слое сырье направляют в каскад из 3 адиабатических реакторов. На установке с движущемся слоем катализатора используют три реактора, выполненных в виде единой конструкции и расположенных один над другим.
В любом варианте исполнения отношение объемов катализатора в секциях составляет 1/2/4. Это связано с тем, что соотношение скоростей дегидрирования, изомеризации и дегидроциклизации составляет 4/2/1.
Основные реакции риформинга.
Основой процесса служат три типа реакций. Наиболее важны реакции, приводящие к образованию Ar у/в.
1. Дегидрирование шестичленных нафтенов:
2. Дегидроизомеризация пятичленных нафтенов:
3. Ароматизация (дегидроциклизация) парафинов:
Другой тип реакций, характерных для риформинга – изомеризация. Наряду с изомеризацией 5-ти членных и 6-ти членных нафтенов изомеризации подвергаются как парафины, так и ароматические у/в.
Способы получения сложных эфиров. Основные продукты и области их применения. Условия проведения реакции этерификации органических кислот со спиртами. Катализаторы процесса. Особенности технологического оформления реакционного узла этерификации.
1. Взаимодействие кислот со спиртами:
![]()
Это наиболее распространенный способ получения сложных эфиров.
2. Синтез сложных эфиров методом конденсации альдегидов:
![]()
Синтез сложных эфиров из альдегидов (реакция Тищенко) осуществляется в присутствии алкоголята алюминия, активированного хлоридом железа или, что лучше, хлоридом алюминия и окисью цинка. Данный метод имеет промышленное значение.
3. Присоединение органических кислот к алкенам:
![]()
4. Синтез сложных эфиров путем дегидрогенизации спиртов:
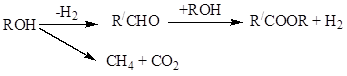
5. Получение сложных эфиров методом переэтерификации.
Данная реакция имеет две разновидности: реакция обмена между эфиром и спиртом спиртовыми радикалами (реакция алкоголиза):
![]()
и реакция обмена кислотными радикалами у спиртовой группы эфира:
![]()
6. Синтез эфиров из ангидридов кислот и спиртов:
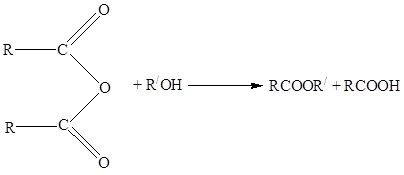
7. Взаимодействие кетонов со спиртами:
![]()
8. Взаимодействие между галоидангидридами и спиртами:
![]()
9. Реакция между серебряными или калиевыми солями кислот и алифатическими галоидными производными:
![]()
10. Взаимодействие кислот с алифатическими диазосоединениями (в основном с диазометаном):
![]()
Основными продуктами реакции этерификации являются сложные эфиры, используемые в качестве растворителей, пластификаторов, синтетических смазочных масел и гидравлических жидкостей, душистых веществ, мономеров.
Этерификацию спиртов карбоновыми кислотами можно проводить в отсутствии катализатора, но в этом случае она протекает медленно и для достижения достаточной скорости требуется высокая температура (200-300О С). Но когда примесь катализатора трудно отмывается, применяют именно некаталитический процесс. В присутствии кислотных катализаторов этерификация протекает при температуре 70-150О С.
Наиболее распространенными катализаторами этерификации являются минеральные кислоты: серная, фосфорная. Могут использоваться бензолсульфокислота, толуолсульфокислота и т.д. Большую группу катализаторов составляют соли органических и неорганических кислот. Могут быть использованы в качестве катализаторов реакции этерификации: перекись титана, молибден на инертном носителе, активный этилат алюминия, алкоголяты титана и др. Все более широкое применение в качестве катализаторов получают ионообменные смолы.