| Скачать .docx |
Реферат: Влияние физических и химических факторов на основность алкиламинов
1.Кислоты и основания
Протон наиболее естественно воспринимается химиком как катион атома водорода"
Р.Белл
В современной химии используются две теории кислот и оснований: теория Бренстеда - Лоури и теория Льюиса - Усановича. Более общие определения кислот и оснований предложены в теории Льюиса - Уеановича. Однако в связи с важной ролью про-толитических процессов в химии теория Бренстеда - Лоури сохранила самостоятельное значение. Именно этой теории мы обязаны появлением комплекса проблем, ставших предметом настоящей книги.
1.1. Теория Бренстеда - Лоури
Согласно теории Бренстеда - Лоури кислота рассматривается как вещество, поставляющее протон, а основание - как вещество, способное присоединять протон (1,2)
![]() А В +Н +
(1)
А В +Н +
(1)
Кислота и отвечающее ей основание, таким образом, образуют сопряженную пару.
Ключевым в теории Бренстеда - Лоури является представление о том, что кислота взаимодействует при переносе протона с другой сопряженной парой (двойное протолитическое равновесие):
![]() А1
+ В2
А2
+ В1
(2)
А1
+ В2
А2
+ В1
(2)
Отсюда вытекают и первые предпосылки для количественного сравнения силы кислот и оснований: сильная кислота отдает протон ”легче”, чем слабая, а сильное основание “крепче” связывает протон, чем слабое. Равновесие тем полнее сдвинуто вправо, чем сильнее кислота А1 и слабее кислота А2 .
Можно представить, что двойное протолитическое равновесие является результатом двух сопряжённых равновесий:
![]() НА Н+
+ А-
(3)
НА Н+
+ А-
(3)
![]() В + Н+
ВН+
(4)
В + Н+
ВН+
(4)
Уравнение (4) лежит в основе количественной теории .позволяющей сравнивать силу различных оснований.
Безусловно, схема кислотно-основного равновесия, сформулированная Бренстедом и Лоури, не полностью отражает истинный процесс. Вернее, уравнение (4) следует считать адекватным процессам, происходящим в газовой фазе, что само по себе достаточно ценно и важно. В растворах же реакция между кислотой и основанием не сводится только к переносу протона от кислоты к основанию. Сначала кислота АН и основание В образуют комплекс АН...В за счет водородной связи между водородом кислоты и электронодонорным атомом основания. Во многих случаях протолитическая реакция преимущественно ограничивается этой начальной стадией комплексообразования. Поэтому такой процесс называется "незавершенным" кислотно-основным равновесием [4]. Следовательно, образование водородных связей рассматривается не только как вспомогательная, переходная ступень при кислотно-основном взаимодействии, облегчающая переход протона от кислоты к основанию, но и как один из самостоятельных видов этого взаимодействия. В благоприятных условиях кислотно-основное взаимодействие не останавливается на стадии комплекса АН...В, и происходит передача протона от кислоты к основанию, в результате чего основание протонируется. Эта вторая стадия цротолитического процесса называется "завершенным" кислотно-основным взаимодействием. При этом образовавшиеся ионы могут находиться в растворе либо в свободном виде, либо в виде ионных пар:
![]()
![]() ВН+
А-
ВН+
| | А-
ВН+
+ А-
, (5)
ВН+
А-
ВН+
| | А-
ВН+
+ А-
, (5)
где ВН+ А- - тесные ионные пары; ВН+ ççА- - сольватно-разделеные ионные пары ; ВН+ и А- -свободные ионы.
Более полным отражением кислотно-основного процесса является следующая схема [4]:
![]()
![]()
![]() АН + В а
АН...В б
А-
...ВН+
в
А-
+ ВН+
, (6)
АН + В а
АН...В б
А-
...ВН+
в
А-
+ ВН+
, (6)
здесь а - незавершенное кислотно-основное равновесие, б - завершенное и в - диссоциация на свободные ионы* . Таким образом, количественное сравнение слабых оснований в рамках теории Бренстеда - Лоури должно осуществляться с учетом реальной ситуации, в которой происходит перенос протона к органическому основанию: в газовой фазе основой для количественных расчетов основности может служить принципиальная схема (4), тогда как в растворах следует опираться на схему (6), а вернее, на ее модификации, учитывающие конкретные условия.
1.2. Физический смысл и меры основности в газовой фазе
Основностью в газовой фазе называют свободную энергию (DG) равновесия (4) [5,6] . Как известно, DG = DН0 - ТDS. Измерения энтропии равновесия в газовой фазе показали, что эта величина обычно не превышает 9-12 Дж/(моль·К). Таким образом, изменение энтальпии равновесия (DН0 ) считается равным (DG0 ) [5].
Изменение энтальпии равновесия (4) переноса протона в газовой фазе, взятое с обратным знаком, называется сродством к протону и обозначается РА (Proton Affinity). Численное значение РА определяется из соотношения:
РА=-DН0 =DН0 (Н+ )+ DН0 (В) - DН0 (ВН+ ) (7)
Где DН0 (Н+ ) - энтальпия образования иона Н+ ; DН0 (В) и DН0 (ВН+) - энтальпия образования основания (В) и его протонированной формы (ВН+ ) соответственно. DН0 (Н+ ) = 1530 кДж. Энтальпии образования органических соединений известны из термохимических справочников или могут быть вычислены по соответствующим эмпирическим формулам [7]. Следовательно, определение сродства к протону РА зависит от возможности определения энтальпии образования протонированной формы основания DН0 (ВН+ ).
Экспериментально определение сродства оснований к протону осуществляется с помощью спектроскопии ионного циклотронного резонанса [8] и масс-спектрометрии высокого давления [5. В настоящее время эти методы позволяют вычислять значения РА с точностью ±0,9 кДж/моль. Таким образом, величина РА является надежным критерием для сравнения основности соединений в газовой фазе.
Существует мнение [5], что на базе значений РА можно построить ”абсолютную”” шкалу основности органических соединений. В последние годы получены значения РА для некоторых алифатических и ароматических аминов, гетероциклических соединений, спиртов, эфиров, альдегидов, кетонов, карбоновых кислот [5] и нитросоединений [9].
2. Основность аминов в газовой фазе
Из рассмотрения данных по основности аминов в растворах следует, что она существенно зависит от электронных и пространственных факторов структуры и сольватации исследуемых соединений. Несмотря на отмеченные успехи при выявлении отдельных зависимостей между основностью и указанными эффектами, до сих нет единого количественного подхода к решению проблемы в целом. Казалось бы, что для оценки влияния строения аминов на их основность наиболее удобными есть соответствующие характеристикистики в газовой фазе, в которой, естественно, сольватационные эффекты отсутствуют. С этой точки зрения большой интерес представляет серия появившихся в последнее время работ (в том числе и обзорных [3, 6, 7, 21,137—140]), в которых обобщены результаты масс-спектрометрических методов, в которых определялись энергии перехода протона между стандартным и рассматриваемым (В) аминами в газовой фазе:
![]() В0
Н+
+ В В0
+ ВН +
(1)
В0
Н+
+ В В0
+ ВН +
(1)
Наличие свободной энергии этого процесса характеризует основность амина В относительно стандарта В0 . Абсолютная основность (В0 ), равная отрицательной свободной энергии (DG0 ) процесса (8), может быть рассчитана, если известно соответствующее
В + Н+ =ВН+ (2)
абсолютное значение для стандартного основания. Энтальпия (DH0 ) процесса (8), взятая с обратным знаком, характеризует сродство аминов к протону (РА) и легко рассчитывается, так как для прото-нирования аммиака, обычно принимаемого за стандарт, она определена независимыми методами [139, 143, 148, 149, 150]. Абсолютные значения 0В и РА* зависят от выбранного стандарта и абсолютной величины РА для него (например, для аммиака значение РА изменяется достаточно широко: 200,7 [139]; 201,4 [151]; 202,3 ± 2,0 [152]; 207 ± 3 [143, 148, 150, 153], 211,3 [149]; 214,4 [45]). Поэтому для выяснения количественных закономерностей влияния структуры аминов на их основность в газовой фазе лучше всего пользоваться величинами DGB (или — dR DG0 [3,7, 47]), когда за стандарт выбран аммиак**.
В табл.1 приведены величины DGB известного к началу 1977 г. ряда аминосоединений. Сопоставление этих данных показывает, что поведение различных аминов как оснований в газовой фазе резко отличается от такового в конденсированных средах. Например, анилин (табл. 1, № 31) в газовой фазе оказался на 6,7 ккал/моль (или почти на 5 ед. рКа ) более основным, чем аммиак (№ 1), в то время как в воде, нитрометане и ацетонитриле (см. выше) наблюдается противоположная ситуация. Аналогичная картина имеет место и для пиридина, который в конденсированной фазе примерно на 4 ед. рКа менее основен, а в газовой фазе (№ 80) на 16 ккал/моль (или ~ на 12 ед. рКа ) более основен, чем аммиак; для ацетамида (№ 32), который в воде ~ на 10 ед. рКа менее основен по сравнению с аммиаком, а в газовой фазе практически равен ему; для пиррола (№ 54) и некоторых других аминосоединений.
Таблица 1. Значения основностиа аминосоеденений в газовой фазеб относительно аммиака
| Номер | Амин | DGBг) | ||
| 1 | NH3 | 0,0 | ||
| 2 | CH3 NH2 | 9,1 | ||
| 3 | C2 H5 NH2 | 11,8 | ||
| 4 | n-C3 H7 NH2 | 13,0 | ||
| 5 | i-C3 H7 NH2 | 14,1 | ||
| 6 | n-C4 H9 NH2 | 13,5 | ||
| 7 | i-C4 H9 NH2 | 14,0 | ||
| 8 | s-C4 H9 NH2 | 15,2 | ||
| 9 | t-C4 H9 NH2 | 16,1 | ||
| 10 | n-C5 H11 NH2 | 13,4д ) | ||
| 11 | t-C5 H11 NH2 | 17,4 | ||
| 12 | n-C6 H13 NH2 | 13,5д ) | ||
| 13 | n-C7 H15 NH2 | 13,6д ) | ||
| 14 | c-C6 H11 NH2 | 16,3 | ||
| 15 | NH2 -NH2 | 3,8 | ||
| 16 | NH2 (CH2 )2 NH2 | 19,0д ) | ||
| 17 | NH2 (CH2 )3 NH2 | 24,5д ) | ||
| 18 | NH2 (CH2 )4 NH2 | 27,1д ) | ||
| 19 | NH2 (CH2 )5 NH2 | 25,4д ) | ||
| 20 | NH2 (CH2 )6 NH2 | 25,4д ) | ||
| 21 | NH2 (CH2 )7 NH2 | 25,2е ) | ||
| 22 | CH3 O(CH2 )2 NH2 | 14,7д ) | ||
| 23 | H2 C=CH-CH2 NH2 | 11,3 | ||
|
HCºC-CH2 NH2 | 6,7 | ||
| 25 | NCCH2 CH2 NH2 | 3,0 | ||
| 26 | CF3 (CH2 )3 NH2 | 10,1 | ||
| 27 | FCH2 CH2 NH2 | 8,0 | ||
| 28 | CF3 (CH2 )2 NH2 | 6,7 | ||
| 29 | F2 CHCH2 NH2 | 4,0 | ||
| 30 | CF3 CH2 NH2 | -1,4 | ||
| 31 | 6,8 | |||
| 32 | CH3 CONH2 | 0,2ж ) | ||
| 33 | HCONH2 | -7,1з ) | ||
| 34 | (CH3 )2 NH | 15,5 | ||
| 35 | CH3 NHC2 H5 | 17,9 | ||
| 36 | (C2 H5 )2 NH | 20,2 | ||
| 37 | (n-C3 H7 )2 NH | 22,2 | ||
| 38 | (i-C3 H7 )2 NH | 23,9 | ||
| 39 | (n-C4 H9 )2 NH | 23,1 | ||
| 40 | (i-C4 H9 )2 NH | 23,6 | ||
| 41 | (s-C4 H9 )2 NH | 25,8 | ||
| 42 | 11,2 | |||
| 43 | 18,0 | |||
| 44 | 20,1 | |||
| 45 | 21,2 | |||
| 46 | 19,2д ) | |||
| 47 | 14,4д ) | |||
| 48 | (H2 C=CHCH2 )2 NH | 19,3 | ||
| 49 | (HCºCCH2 )2 NH | 11,7 | ||
| 50 | NCCH2 NHCH3 | 2,7з ) | ||
| 51 | CF3 CH2 NHCH3 | 6,2з) | ||
| 52 | 12,9 | |||
| 53 | 15,3ж) | |||
| 54 | 4,0ж) | |||
| 55 | NHMe-C=O H |
1,7 | ||
| 56 | (CH3 )3 N | 20,0 | ||
| 57 | (CH3 )2 NC2 H5 | 22,4 | ||
| 58 | (C2 H5 )2 NCH3 | 24,6 | ||
| 59 | (C2 H5 )3 N | 26,7 | ||
| 60 | (C3 H7 )3 N | 28,7 | ||
| 61 | 17,1и) | |||
| 62 | 8,1и) | |||
| 63 | 24,3 | |||
| 64 | 25,7 | |||
| 65 | 27,1 | |||
| 66 | 26,1к) | |||
| 67 | (CH3 )2 N-NH2 | 15,2 | ||
| 68 | ((CH3 )2 NCH2 )2 | 30,3 | ||
| 69 | 23,5 | |||
|
||||
70 |
(H2 C=CH-CH2 )3 N | 24,7 | ||
| 71 | (HCºC-CH2 )3 N | 15,0 | ||
| 72 | NCCH2 N(CH3 )2 | 7,1 | ||
| 73 | F3 CCH2 N(CH3 )2 | 20,9 | ||
| 74 | 19,5 | |||
| 75 | 21,0ж ) | |||
| 76 | 23,7ж ) | |||
| 77 | 19,3 | |||
| 78 | 21,8 | |||
| 79 |  |
26,0 | ||
| 80 | 16,0 | |||
| 81 | CH3 CON(CH3 )2 | 11,7 | ||
| 82 | HCON(CH3 )2 | 7,6 | ||
| 83 | NF3 | -56л) |
Существенные различия между свойствами в газовой и конденсированной фазах наблюдается и при сравнении оснований одного и того же класса. Например, все первичные алкиламины в газовой фазе (№2—29), за исключением b,b,b-трифторэтиламина (№30), оказались более основными, в то время как в воде (см. например, табл. 1) амины с электроотрицательными заместителями зачастую менее основны, чем аммиак. То самое относится и ко вторичным и третичным алкиламинам.
Данные по изменению свободной энергии и энтальпии реакций, описываемых уравнениями (17) — (2), совместно с некоторыми другими результатами позволили определить термодинамические характеристики процессов переноса свободных и протонированпых оснований из газовой фазы в водные растворы и на этой основе про вести термодинамический анализ влияния сольватации на основность аминов в воде [3, 6, 47, 140, 151, 153]. При этом преимущественное внимание было уделено причинам, обусловливающим наблюдаемый порядок изменения основностии в воде при переходе от аммиака к первичным, вторичным и третичным алкиламинам с насыщенными углеводородными заместителями. На основе этих данных Ариетт с сотрудниками [3, 6, 47] сделал вывод, что главным фактором, определяющим наблюдаемый порядок основности аминов различных классов в воде, является специфическая сольватация соответствующих катионов, зависящая от числа атомов водорода у протонированного азота. Неспецифическая же сольватация, по их мнению, имеет второстепенное значение, т. е. эти исследователи придерживаются сольватационной (гидратационной) теории Тротмана — Диккенсона (см. выше).
В то же время другая группа исследователей [140, 153] считает, что изменение основности аминов при переходе из газовой фазы в воду обусловлено прежде всего электростатической (неспецифической) сольватацией катионов, а специфическое взаимодействие играет второстепенную роль. При этом в указанных работах принимается, что кислотно-основные свойства соединений в газовой фазе являются истинными (собственными) свойствами, и в противоположность случаю в конденсированной фазе практически не обсуждается зависимость этих свойств от строения аминов.
Следует отметить, что, несмотря на большой интерес, проявляемый к результатам по основности аминосоединеиий в газовой фазе, пока еще нет общего подхода к объяснению эффектов их структуры на данное свойство. Выявлены только некоторые закономерности, характеризующие поведение отдельных групп родственных аминов. Например, Тафт рассмотрел изменение основности при переходе от аммиака к первичным, вторичным и третичным аминам и нашел, что введение одной, двух или трех алкильных групп (СН3; С2 Н5 ; n-С3 Н7 ; Н2 С=СН—СН2 ; НСЕºС—СН2 ) сопровождается ростом величин DGB в соотношении 1,00 : 1,72 : 2,22. Повышающее основность действие метильных групп при последовательном накоплении их в a-положении может быть представлено пропорциональностью 1,00: :1,85 : 2,60 [7]. Введение метильной группы в a-положение увеличивает основность амина примерно на 2,1 ккал/моль, в b-и g-положения — на 0,9 и 0,5 ккал/моль соответственно [155].
При сопоставлении ароматических и алифатических аминов с одинаковым числом углеродных атомов у атома азота было найдено, что изменение гибридизации a-атомов углерода (например, переход от пиридина к N-метилпирролидину, от анилина к циклогексиламину) практически одинаково влияет на изменение основности в воде и газовой фазе [7]. Была также обнаружена приблизительно прямолинейная зависимость между изменениями основности аминосоединений, имеющих одинаковое число углеродных атомов у азота, но разный характер гетероатома, и степенью этой гибридизации [159], а также между основностью алкиламипов и степенью гибридизации b-углеродного атома в алкильном радикале [7]. В тех случаях, когда варьирование заместителя происходит не у реакционного центра, были выявлены более строгие закономерности влияния структуры на основность аминов. Так, найдена корреляция между DGB для a-замещенных триметиламинов и sI этих заместителей [7]. Величины DGB для 3-й 4-замещенных пиридинов хорошо коррелируют [7, 162, 163] с их основностью в воде и с постоянными sI (s°) и sR + (sG + ) характеризующими электронные эффекты заместителей [7, 158, 163]. Аналогичные зависимости (но менее строгие) можно получить и при подобных сопоставлениях основности замещенных анилинов в газовой фазе [3, 7].
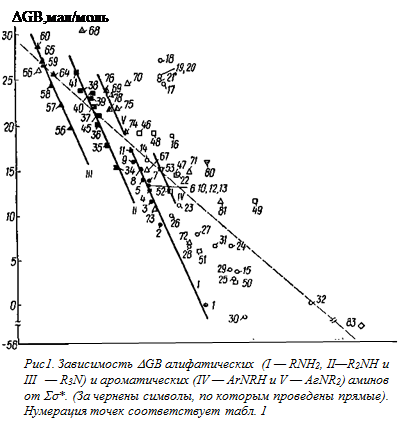 Непосредственное сравнение величин DGB (см. табл. 1) со значениями Ss* заместителей*
, присоединенных к атому азота, показывает что, на первый взгляд, здесь отсутствует какая-либо зависимость. Тем не менее имеется некоторая тенденция к уменьшению основности рассматриваемых соединений с ростом электро-отрицателыюсти заместителей в них. Это позволило через 40 (из 47) точек для различных аминосоединений (алкиламины, ариламины, производные гидразина и амиды), основности которых в газовой фазе были известны к концу 1974 г., провести прямую, описываемую [158] уравнением**
Непосредственное сравнение величин DGB (см. табл. 1) со значениями Ss* заместителей*
, присоединенных к атому азота, показывает что, на первый взгляд, здесь отсутствует какая-либо зависимость. Тем не менее имеется некоторая тенденция к уменьшению основности рассматриваемых соединений с ростом электро-отрицателыюсти заместителей в них. Это позволило через 40 (из 47) точек для различных аминосоединений (алкиламины, ариламины, производные гидразина и амиды), основности которых в газовой фазе были известны к концу 1974 г., провести прямую, описываемую [158] уравнением**
DGB = (2,1±0,1) — (6,46±0,16)Ss*, (s = 2,1; r = 0,988). (3)
Если аналогичную прямую (пунктирная линия на рис. 4) провести через каждую 71 точку, представленную на указанном рисунке, то ее уравнение имеет вид
DGB = (23,9 ± 0,7) — (8,94 ± 0,48) Ss*,
(s = 4,73; r =0,914). (4)
Следует отметить, что в этом случае при сравнительно узких доверительных интервалах в параметрах уравнения (20) на рис. 4 наблюдаются довольно значительные отклонения от указанной прямой/
Например, точка для аммиака (№ 1) отклоняется вниз, а для тетра-метилендиамина (№ 18) — вверх почти на 11 ккал/моль. Более того, и так невысокий (0,914) коэффициент корреляции значительно уменьшается (до 0,798) при исключении из рассмотрения далеко отстоящей точки для №3 (№ 83). Поэтому найденную зависимость (уравнение (4)), вероятно, можно рассматривать как качественное соотношение, отражающее указанную выше тенденцию к уменьшению DGB с ростом электроноакцепторности заместителей в аминосоединеииях.
Интересные результаты получаются при рассмотрении величин DGB для алкиламинов с насыщенными углеводородными радикалами. Как видно из рис. 4, соответствующие точки (полностью зачерненные символы) группируются таким образом, что для первичных, вторичных и третичных аминов можно провести отдельные прямые [164] с наклонами, соответственно равными: —22,8 ± 2,2; —23,9 ± 2,7 и —23,5 ± 2,2.
Наличие отдельных прямых для алкиламинов различных классов не является неожиданностью. Так, при подобной обработке (сопоставление с Ss*) потенциалов ионизации — одной из важнейших составляющих сродства к протону в газовой фазе [47, 151, 153]) — было найдено [165], что по аналогии с корреляцией потенциалов ионизации различных органических соединений Rx МНy (где М =С, О и S) эти данные лучше всего представлять в виде отдельных зависимостей для первичных, вторичных и третичных аминов, хотя имеется и другой подход, в соответствии с которым зависимость потенциалов ионизации аминов от их структуры описывается единым уравнением [166]. Однако первый подход более предпочтителен, поскольку он охватывает больший набор аминов, а также рассматривает с единых позиций потенциалы ионизации самых различных соединений* . Кроме того, при сопоставлении величин РА с потенциалами ионизации [153, 155] и энергиями связывания остовных (1s) электронов [167] наблюдается также отдельные прямые для разных классов аминов. Следует отметить, что при сравнении термодинамических характеристик процессов протонирования аминов в газовой и конденсированной фазах, общей и электростатической теплот гидратации алкиламмоний-ионов как с величинами РА, так и с радиусами этих ионов были получены отдельные прямые для первичных, вторичных и третичных аминов [3, 140, 153]. При этом амины с электроотрицательными заместителями в тех случаях, когда соответствующие данные рассматривались, заметно отклонялись от найденных зависимостей [140]. Из рис. 1 отчетливо видно, что точки (незачерненные символы) для аминов, содержащих электроотрицательные заместители, отклоняются (иногда существенно) от полученных прямых, т.е. здесь наблюдается то же явление, что и при сопоставлении величин DН протонирования аминов в воде и газовой фазе.
Отклонения, наблюдаемые для диаминов (табл. 1, № 16—21), обусловлены внутримолекулярной сольватацией типа III [156,157]. Влияние этой сольватации, которое можно количественно оценить по отклонению соответствующих точек от прямой I на рис. 4, сильнее всего проявляется при n = 4, что можно связать с устойчивостью соответствующих структур.
Внутримолекулярная сольватация того же типа, вероятнее всего, ответственна и за отклонения вверх точек для b-метоксиэтиламина (№ 22), пиперазина (№ 46), морфолина (№ 47) и N,N-тетраметилэтилендиамина (№ 68) от соответствующих прямых. В случае диазобициклооктана (№ 69) существенное отклонение (~ 13 ккал/моль) точки о! прямой для третичных аминов, вероятно, обусловлено стабилизацией его катиона за счет взаимодействия неподеленной электронной пары непротонированного атома азота с орбиталым атомом азота, к которому присоединен протон.
 |
Отклонения точек для аминов, содержащих электроотрицательные заместители, также, по-видимому, следует связывать с увеличением DGB этих аминов за счет стабилизации их катионов при образовании внутримолекулярных водородных связей, например типа IV для фторсодержащих алкиламинов.
Труднее объяснить наблюдаемые отклонения от соответствующих прямых точек для циклогексиламина (№1 4), гидразина (№ 15), манксина (№ 66) и N,N-диметилгидразина (№ 67). Здесь, по-видимому, проявляется как некоторое расхождение в величинах GB, полученных разными авторами (например, в случае манксина приведенное в табл. 1 значение DGB было рассчитано при сопоставлении данных по РА этого амина и GB других аминов), так и влияние (в гидразинах) неподеленной электронной пары на α-гетероатоме (α-эффект ).
При рассмотрении основности ароматических аминов в газовой фазе (табл. 1, № 31, 52, 53,74—78), прежде всего обращает внимание тот факт, что их величины DGB значительно выше, чем для аммиака, и практически совпадают с таковыми для алифатических аминов с насыщенными углеводородными заместителями. Такое аномальное поведение анилина и его производных объясняется повышенным влиянием поляризуемости фенильного кольца в газовой фазе, которое превышает действие резонансного эффекта. Указанное влияние поляризуемости α-непредельных связей проявляется и в случае дифенил- и трифениламинов. Так, трифениламин, основность которого в воде не поддаётся измерению в газовой фазе,оказался сильнее, чем даже метиламин. Повышена основность и дифенилами на, который по своему сродству к протону в газовой фазе находится между метиламином и анилином. Используя отданные, можно попытаться количественно оценить различие во влиянии поляризуемости и резонанса фенильной группы на основность ариламинов. Для анилина, где соответствующая величина расчитывалась как отклонение его точки от корреляционной прямой для первичных алкнламинов, она оказалась равной примерно 10 ккал/моль. В случае дифениламина (отклонение от прямой для вторнчных алкиламинов) при использовании среднего значения DGB между анилином и метиламином (~ 8 ккал/моль) получается, что действие каждой фенильной группы равно ~ 10 ккал/моль. А для трифениламина (DGB = ~ 11 ккал/моль как среднее значение между метиламином и М-метиланилином данная величина, определенная по отклонению от прямой для третичных алкиламинов, оказа лась равной ~ 11 ккал/моль. Таким образом, можно считать, что; различие в действии эффектов поляризуемости и резонанса
каждой α-кратной связи практически не зависит от числа таких связей.
Влияние только резонансного эффекта количественно оценивается при сравнении основности в газовой фазе бензохинуклиди-1 на (№ 79) и N,N-диалкиланилинов (№ 74—78). Сопоставление значений DGB для этих аминов приводит к величине ~ 5 ккал/моль, Принимая во внимание отмеченное выше различие во влиянии поляризационного и резонансного эффектов фенильных групп, можно считать, что эффект поляризуемости α-непасыщеной связи на газофазную основность аминов равен ~ 15 ккал/моль.
Вероятно, вследствие проявления эффектов поляризуемости пиррол (№ 54 в газовой фазе из-за повышающего основность влияния двух α-кратных связей оказался основнее аммиака на 4 ккал/моль.
Влияние поляризуемости, по-видимому, является ответственным за значительное повышение основности газовой фазе пиридина (№ 80) амидов* (№ 32, 33, 55, 81, 82) по сравнению с аммиаком и алкил- аминами.
Рассмотренные данные показывают, что влияние поляризуемости непредельных группировок на основность аминов в газовой фазе оказывается весьма эффективным (оно значительно превышает резонансные влияния). В то же время поляризуемость насыщенных радикалов, которая должна увеличивать основность соединения с ростом числа заместителей у реакционного центра в данном случае практически не проявляется, поскольку третичные алкиламины являются более слабыми основаниями, чем вторичные и первичные при равных величинах Σσ*(ср. расположение прямых I - III на рис. 1).
Интересно сопоставить основность в газовой фазе трехфтористого азота (см. № 83 в табл.1) и аммиака (№ 1). Пониженная основность NF3 в первом приближении может быть объяснена акцепторным действием трех атомов фтора у азота. Однако при количественном рассмотрении получается, что с учетом величины Σσ* атомов фтора значение ΔGB для этого соединения должно быть равным примерно — 190 ккал/ моль. Повышение наблюдаемой величины над расчётной (примерно на 130 ккал/моль) трудно объяснить на основе любых известных эффектов атомов фтора. Однако возможно, что здесь протоиирование осуществляется не по атому азота, а по атом у фтора. В пользу этого может свидетельствовать тот факт, что величины РА для НF, СН3 F и С2 Н5 F равны 137, 151, 163 ккал/моль соответственно, т. е. практически совпадают со значением для NF3 (151 ± 10 ккал/моль ).
Следует отметить, что влияние алкильных заместителей у атома азота в анилине оказывается аналогичным таковому для алифатических аминов, т. е. основность их увеличивается с ростом числа и размера радикалов (ср. № 31, 52, 53, 74—78), и это влияние удовлетворительно описывается уравнением типа (1). Из рис. 1 видно, что точки (частично зачерненные символы) для N-алкил- и N,N-Диалкиланилинов ложатся на отдельные прямые практически с тем же наклоном, что и для алифатических аминов.
В связи с тем, что наклоны прямых па рис. 1 для алифатических и ароматических аминов практически совпадают, все рассмотреные данные для 34 аминов были обработаны по единому уравнению. В соответствии с этими расчетами влияние структуры названных аминов описывается следующими уравнениями
DGB = 32,7 ± 0,2 — 23,1 ± 0,З Σσ* (первичные алкиламины), (5а)
DGB = 27,6 ± 0,3 — 23,1 ± 0,3 Σσ* (вторичные алкиламины), (56)
DGB = 20,3 ± 0,3 — 23,1 ± 0,3 Σσ* (третичные алкиламины), (5в)
DGВ = 38 ± 0,5 — 23,1 ± 0,3 Σσ* (N-алкиланилины), (5 г)
DGB = 32,6 ± 0,4 — 23,1 ± 0,З Σσ* (N,N-диалкиланилины), (5д)
(s-0,731, R = 0,990).
При этом оказалось, что первичные алифатические и третичные ароматические амины случайно ложатся практически на одну и ту же линию (прямые I и V на рис. 1). Величина ρ* (~ — 17, если перевести ее в размерность рКа ) здесь оказалась значительно выше, чем для воды (~-3) и других заместителей.
Расположение прямых на рис. 4 свидетельствует о том, что в газовой фазе сродство аминов к протону при равенстве Σσ* их радикалов изменяется в ряду: первичные> вторичные> третичные
В+ Н · (Н2 О)п-1 + Н2 О « В+ Н • (Н2 0)n (6)
Эти данные свидетельствуют о том, что, например, кластер |МН4 (Н2 0)4 практически не обладает особой устойчивостью по сражению с кластерами другого состава, поскольку на графиках «свойство — n» (n изменяется от 1 до 5) некоторый излом при N = 4 обнаруживается только при рассмотрении изменений энтальпии процесса В случае изменений свободной энергии [180] никакого излома не наблюдается, хотя при преимущественном образовании первого гидратного слоя в соответствии с рассмотренной, выше сольватационной теорией следовало бы ожидать различный характер обеих указанных зависимостей в области n < 4 (образование первого гидратного слоя) и n > 4 (образование следующего слоя), т. е заметные изломы при n = 4 Для катиона триметиламмония соответствующий график как для DH°, так и для DG° не претерпевает никаких изменений при любых n (от 1 до 5) Аналогичная монотонная зависимость соблюдается при любых n [от 1 до 8) при гидратации протона в газовой фазе.
Таким образом, рассмотрение закономерностей влияния структуры аминов на их основность в газовой фазе показало, что эго влияние оказалось не проще, чем в конденсированной, а даже несколько сложнее, поскольку здесь наряду с эффектами, действующими в растворах, проявляются и другие факторы. Поэтому использование величин GB или РА, являющихся, по мнению Арнетта, “наиболее подходящей характеристикой основности”, для оценки влияния строения аминосоединений на их свойства и эффектов сольватации из-за сложности учета всех указанных факторов в настоящее время пока затруднительно. Тем не менее выявленные закономерности дают основание полагать, что с накоплением нового экспериментального материала положение в этой области существенно прояснится.
Удалось показать, что значения РА подчиняются принципу линейности свободных энергий (ЛСЭ). Так, при изменении свойств заместителя в g-положении пиридинового цикла наблюдаются хорошо коррелирующие зависимости с электронными константами si и sr + (10)
РА/РА0 = 1б,7sI + 10 , 3 sr + (8)
где РА° и РА - сродство к протону пиридина и пиридина, замещенного в g -положении. Интересно, что основность пиридинов в газовой фазе в большей степени чувствительна к электронным эффектам заместителей, чем в водном растворе. Более подробно причины этих различий, которые часто принимают характер инверсии, будут обсуждаться дальше. Здесь же отметим, что основность соединения в соответствии со схемой (4) определяется разностью свободных энергий нейтральных молекул и соответствующих протежированных форм. Бри этом главный вклад в энергетический баланс вносит стабильность ионов BН+ .
Ионы в газовой фазе не стабильны. Раз образовавшись, они быстро гибнут в результате рекомбинации с ионами противоположного знака или на стенке [5]. Наиболее неустойчивы в газовой фазе простейшие ионы Н3 0+ , NН4 + . В жидкой среде ионы стабилизируются за счет сольватации, энергия которой может превысить энергию образования иона из молекулы. В этом случае можно ожидать инверсии основности при сопоставлении данных в газовой фазе и в растворе. Строение многих слабых органических оснований способствует делокализации образовавшегося при протонировании заряда. Такие ионы стабильны в газовой фазе, а основность соответствующих оснований при прочих равных условиях будет выше. Именно возможностью делокализации положительного заряда в анилиниевом ионе объясняется более высокая по сравнению с аммиаком основность анилина в газовой фазе, тогда как в воде аммиак - значительно более сильное основание, чем анилин [5,11].
Таким образом, эксперименты в газовой фазе позволяют выдвинуть критерий сравнения основности соединений (в том числе и слабых оснований), проследить влияние на основность заместителей в реакционных сериях. Во всех подобных случаях в качестве такого критерия рассматривается сродство к протону РА. Однако экспериментальная техника определения РА пока еще чрезвычайно сложна и недоступна для большинства химических лабораторий. Кроме того, в сложных случаях, когда возможно присоединение протона к более чем одному центру основности соединения (а такие ситуации - отнюдь не редкость), интерпретация полученных экспериментально параметров вызывает существенные затруднения. 3 связи с этим были предприняты попытки установления линейных зависимостей между РА и другими параметрами, более доступными экспериментально и адекватно отражающими сложный характер протонирования.
В работах [12, 13] одновременно и независимо предложена линейная зависимость между РА и энергией ионизации для кислород- и азотсодержащих оснований:
РА = - IЕ(Х1s
) + const (9)
где IЕ(Х1
s
) - энергия ионизации для 1s-электрона центра основности - атома кислорода (X = 0) или азота X = М). Теоретическое обоснование зависимости (9) базируется на сходстве моделей протонизации и удаления 1s-электрона при ионизации, И в
том и в другом случае энергия может быть выражена суммой двух членов (термов): один терм связан с электронной плотностью на орбитали, ответственной за ионизацию (initial state), другой - со стабилизацией заряда после ионизации (final state).Заместители могут оказывать влияние как на первый терм (индуктивный эффект), так и на второй (поляризационный эффект), причем последний в случав органических оснований обычно преобладает в обеих моделях ионизации [13]. Вместо IЕ в уравнении (9) было предложено использовать потенциал ионизации (IР) [13,14]. По мнению авторов, применение величины IР*
более корректно в случае сложных органических молекул, направление протонизации в которых может быть неоднозначным. В работе [13] приведены корреляционные соотношения между РА и IР и, в частности, для карбонильных соединений (РА = -0,690 IР + 15,03) и для спиртов и эфиров (РА = - 0,397 IР + 12,29). Подводя итог рассмотрению экспериментальных исследований процесса переноса протона в газовой фазе, отметим, что найденные в этих работах критерии полезны и пригодны для количественного сравнения основности в данных условиях*. Более того, из сопоставления экспериментальных данных, полученных для одних и тех же соединений в газовой фазе и в растворе, могут быть выполнены количественные оценки энергии сольватации про тонированных оснований. В основу таких расчетов положен термодинамический цикл Борна [б].
Однако довольно часто при изучении протонирования органических оснований возникает необходимость установить центр присоединения протона. В тех случаях, когда органическая молекула обладает несколькими вероятными центрами основности, не всегда можно предугадать, куда именно присоединится протон. При этом весьма желательно иметь наглядное представление об изменении электронной структуры и конфигурации молекулы в результате протонирования. Как правило, экспериментальные метода не дают однозначного ответа на эти вопросы. Кроме того, некоторые зависимости, установленные экспериментально, например (8), (9), нуждаются в теоретической интерпретации. В этих случаях на помощь приходят квантово-химические методы исследования.
3. Закономерности, выявленные для основности
Наличие свободной электронной пары у атома N придаёт аминогрупам основные свойства. В соответствии с теорией Брауна. Основание является акцептором протона: образуется протонированная форма амина. Согласно определению Льюиса, атом может образовывать связь с кислотами Льюиса, т. е. С любыми частицами, имеющими орбиталь, способную принять участие в создании связи с использованием электронной пары основания.
![]() R3
N:
+ AH R3
N+
H + A-
(1)
R3
N:
+ AH R3
N+
H + A-
(1)
Равновесие кислота — основание устанавливается довольно быстро, и при обсуждении основности следует рассмотреть положение равновесия в данной системе. Оно определяется разностью свободных энергий DG0 основания и сопряженной кислоты. На относительную устойчивость этих двух частиц влияют три основных фактора: электронные факторы, природа растворителя и структурные особенности, которые будут рассмотрены ниже.
Влияние электронных факторов на основность можно оценить с помощью данных об основности в газовой фазе, полученных рядом методов, таких, например, как масс-спектрометрия или ионный циклотронный резонанс. Эти методы позволяют изучать ион-молекулярные взаимодействия и рассчитывать DG0 по уравнению 3, где GB — основность в газовой фазе,
![]() АН+ВВН + А(2)
АН+ВВН + А(2)
DG0
= GB(А)-GB(В)(3)
Результаты, полученные при изучении большого числа алкиламинов, были использованы для количественной оценки влияния алкильных групп на основность самих аминов. Порядок возрастания этого влияния согласуется с увеличением электронодонорного «индуктивного эффекта» алкильных групп, который оказывает сравнительно более сильное стабилизующее воздействие на протонированные формы аминов, чем на свободные амины. В соответствии с этим наблюдается увеличение основности, например, в следующем ряду:
NН3 < МеNН2 < ЕtNН2 < н-BuNН2 < Ме2 NН < Ме3 N < Еt3 N < н-Вu3 N
Понятие “индуктивный эффект” достаточно хорошо обосновано экспериментально и является очень полезным для химиков-органиков, однако стало очевидным, что алкильные группы способны стабилизовать не только положительные, но и отрицательные ионы. Это следует из характера кислотности спиртов в газовой фазе (ВuОН > EtOН > МеОН > Н2 О) и влияния алкильных заместителей на увеличение силы кислоты в растворе. Этот эффект можно представить как результат делокализации .положительного или отрицательного заряда в молекуле вследствие поляризации различных связей. Как и следует ожидать, .электроотрицательные атомы понижают основность, например, в ряду:
СН3 СН2 NН2 > FСН2 СН2 NH2 > F2 СНСН2 NН2 > F3 ССН2 NH2
Оценка основности в газовой фазе относительно аммиака
![]() NH4
+ B NH3
+ BH
NH4
+ B NH3
+ BH
DG0 = GB(NH3 ) - GB(В)
Таблица 2. Основность некоторых аминов в газовой фазе
| соединение | DG0 , кДж/моль | соединение | DG0 , кДж/моль |
 |
-101,7 |  |
-75,0 |
 |
-103,0 | -46,9 | |
 |
-84,2 | -64,9 | |
 |
-84,6 | -28,1 | |
 |
-75,4 | -47,3 | |
| -54,4 |
дала возможность сравнить циклические и ациклические амины (табл. 1); важно отметить, что для аминов, имеющих аналогичные заместители, значения DG0 близки (отрицательные значения указывают на большую силу основания). Отклонение, наблюдаемое в случае азиридина, находит объяснение в рамках теории гибридизации: орбиталь свободной электронной пары в азиридине носит более выраженный s-характер, чем в диметиламине, и поэтому менее вероятно ее участие в образовании связи с протоном. Для бензиламинов, по-видимому, экспериментальных данных недостаточно; для трех первичных аминов, представленных в табл. 1, наблюдается удовлетворительная корреляция между характером гибридизации b-углеродного атома и значением DG0 .
Закономерности, выявленные для основности различных аминов в газовой фазе, привлекают своей простотой и четкостью. Большинство экспериментов в органической химии осуществляется в растворах, и в этих случаях изменение основности может иногда описываться приблизительно такими же закономерностями, как и в случае газовой фазы (например, Bu3 > Вu2 NН > ВuNН2 , полученный для растворов в хлорбензоле относительно 2,4-динитрофенола). Однако часто эти выводы не носят общего характера; так, в бензоле наблюдается следующий порядок основности: Вu2 NН > Вu3 Н > ВuNH2 . В течение многих лет химики проявляли особый интерес к закономерностям, существующим в водных растворах. В этом случае основным параметром является свободная энергия протонирования основания в воде DG0 (Н2 О), выражаемая обычно как рKа сопряженной кислоты + ВН [DG0 (Н2 О) = —RТlnКа] - Значения рKa для простейших аминов приведены в табл. 2.
Таблица 2. Значение рКа кислот, сопряжённых с алкиаминами (Н2 О, 25 0 С)
| Соединение | рКа | |
| R=Et | R=Me | |
| R3 N | 10,85 | 9,80 |
| R2 NH | 11,09 | 10,73 |
| RNH2 | 10,80 | 10,66 |
| NH3 | 9,25 | |
Отсутствие четкой закономерности в поведении алкиламинов, объясняли по-разному. Влияние пространственных факторов на стадии протонирования можно не учитывать, и долгое время признавалась важность эффектов сольватации, протекающей в различной степени. Недавно Ауэ применил эти данные в сочетании с известными термодинамическими параметрами в водных растворах для всестороннего анализа дифференциальной сольватации [142]. В ряду алкиламинов теплоты гидратации обычно закономерно понижаются с увеличением размеров молекул. Это влияние алкильных заместителей, называемое гидрофобными эффектами, изучено недостаточно, однако предполагают, что подобные эффекты почти полностью отсутствуют в нейтральных и протонированных аминах, находящихся в водной системе. Считают, что в растворе важным фактором является влияние на сопряженную кислоту ослабления взаимодействия между растворителем и протонированным амином при делокализации заряда в ионе. К тем же выводам приходят при интерпретации этого явления с точки зрения электростатической сольватации (считают, что энергия сольватации и ионный объем связаны обратной зависимостью) и сольватации с участием специфических водородных связей (при этом каждая специфическая водородная связь ослабляется вследствие делокализации положительного заряда в ионе). Таким образом, в тех случаях, когда усиление поляризуемости вследствие увеличения числа алкильных заместителей приводит к стабилизации иона аммония за счет делокализации заряда, сольватация иона должна происходить менее экзотермично, способствуя ослаблению стабилизующего влияния заместителей по сравнению с тем, что имеет место в газовой фазе. Поэтому в ряду алифатических аминов суммарное влияние увеличения степени алкилирования постепенно ослабевает и может фактически приводить к обращению ряда в тех случаях (например, Ме3 N в табл. 2), когда эффект уменьшения стабилизации при сольватации сильнее, чем внутримолекулярное стабилизующее влияние алкильных заместителей. И, наоборот, в тех случаях, когда индуктивные эффекты могут вызывать дестабилизацию иона аммония, ион будет обладать повышенной плотностью заряда на атоме азота и лучше сольватироваться; здесь вновь наблюдается противодействие электронным эффектам. Важность сольватации можно подчеркнуть тем, что изменение свободной энергии при переходе ионов аммония из газовой фазы в водный раствор может составлять до 25— 110 кДж/моль (примерно аналогично изменению DG0 за счет электронных эффектов алкильных заместителей в газовой фазе). Для более подробного и систематического знакомства с термодинамическим аспектом данной проблемы и уяснения природы эффектов сольватации читателю следует обратиться к работам [140—142].
В данном разделе не будет дублироваться обсуждение явления постепенного понижения основности при переходе от алкиламинов к аридаминам и амидам. Понижение основности по мере усиления s-характера азота (например, в пиридине и нитрилах) также освещается в соответствующих разделах.
Как уже отмечалось, данные, говорящие о каком-либо влиянии пространственных факторов на перенос протона в газовой фазе, отсутствуют, но при описании взаимодействия аминов с кислотами Льюиса (уравнение 4) становится важным учет объема заместителей. Этот фактор впервые был рассмотрен в классическом исследовании Брауна:
![]() R3
N + BMe3
R3
N ® BМe3
(4)
R3
N + BMe3
R3
N ® BМe3
(4)
Сравнение теплот диссоциации комплексов аминов с кислотами Льюиса и теплот диссоциации соответствующих аммониевых ионов позволяет достаточно точно оценить энергию пространственного напряжения, которое наблюдается у аминов, содержащих заместители различного объема (табл. 3).
Таблица 3. Энергия пространственного напряжения для аддуктов и триметилбора.
| Амин | Энергия пространственного напряжения | Амин | Энергия пространственного напряжения |
| Me2 NH | 5,9 | Et2 NH | 30,1 |
 |
12,1 | Трет-BuNH2 | 33,5 |
| 18,1 | Et3 N | 71,2 | |
| 29,3 |
Измерение констант равновесия дает сведения о собственной основности ряда аминов, для которых пространственные факторы не меняются, а изменение заместителей происходит на большем удалении от атома азота. Были изучены многие другие комплексы аминов, например комплексы с ионами металлов, комплексы с лантаноидными элементами); с галогенами и полинитросоединениями, включая пикриновую кислоту. Реакция образования пикратов лежит в основе классического метода идентификации аминов.
Аминогруппы обладают способностью к внутри- и межмолекулярной ассоциации друг с другом или с другими функциональными группами. Оба возможных типа водородной связи (амин выступает как донор водорода или как акцептор) иллюстрированы формулами (5) и (6). Термином “водородная связь” в каждом случае принято обозначать более слабую из двух связей с водородом.
![]()
(5)
![]()
(6)
Образование водородных связей происходит в твердом состоянии, в жидкой фазе, в растворе, а иногда даже и в газовой фазе. По прочности водородная связь (~8— 40 кДж/моль) является промежуточной между ковалентными и ван-дер-ваальсовыми связями Особая важность этого типа связи была продемонстрировала в ходе обсуждения основности в водном растворе. Определенное влияние водородных связей на физические свойства выражается в том, что температуры кипения первичных аминов выше, чем температуры кипения углеводородов приблизительно той же молекулярной массы, хотя в случае третичных аминов этот эффект, естественно, исчезает. Были изучены спектроскопические проявления водородной связи; эти наблюдения лежат в основе способов ее обнаружения и изучения. Проблеме водородной связи посвящены краткие обзоры [143] и обширные монографии [144].
* для равновесия в возможна более сложная картина, предусмотренная схемой (5)
* К сожалению, на рис. 1 не нанесён ряд точек из-за отсутствия или неточности, на наш взгляд, величин s* для заместителей в некоторых аминах.
** В качестве стандартного основания был выбран триметиламин, а величина r* дана в ед. рКа .
* Найденные в работах [165, 166] корреляционные зависимости качественно не изменяются, если вместо рассмотренных в них адиабатических потенциалов ионизации воспользоваться данными по вертикальным потенциалам ионизации [155].
* Сравнение величин DGB для амидов и аминов основано на допущении, что амиды в газовой фазе протонируются по атому азота. Однако этот вопрос, как и в случае водных растворов, (см. выше) пока ещё не решён.
* Значения IР могут быть определены экспериментально с помощью метода фотоэлектронной спектроскопии или вычислены путём квантово-химических расчётов.