| Скачать .docx |
Курсовая работа: Устройства функциональной электроники
Федеральное агентство по образованию
Государственное образовательное учреждение высшего профессионального образования
Тульский государственный университет
Кафедра радиоэлектроники
Устройства функциональной электроники
Выполнила: Жуковская М.А.
гр. 151371
Проверил: Миронов М.М.
2011 г.
Содержание
Глава 1. Физико-химические основы зарождения и роста новой фазы
1. Анализ гомогенного и гетерогенного зарождения новой фазы
2. Влияние технологических факторов зарождения новой фазы на структуру пленок
3. Рост пленок. Эпитаксия
4. Химический рост эпитаксиальных пленок
Глава 2. Физико-химические основы поверхностных процессов
1. Термодинамика поверхностных процессов
2. Адсорбционные процессы на поверхности твердых тел
3. Факторы, влияющие на адгезию
4. Процессы очистки, промывки и пропитки поверхности
5. Электрофизические характеристики соприкасающихся поверхностей и границ раздела слоев
Глава 1. Физико-химические основы зарождения и роста новой фазы
1. Анализ гомогенного и гетерогенного зарождения новой фазы
Пленки металлов, диэлектриков и полупроводников, осажденные на различные поверхности, используют в электронной аппаратуре как функциональные элементы резисторов, конденсаторов, транзисторов, ИМС, ПП, а также различных приборов на акустических поверхностных волнах и магнитных доменах, с зарядовой связью и др. Кроме того, пленки применяют при изготовлении покрытий, обеспечивающих высокие потребительские (эстетические) качества РЭА.
Механизм процессов зарождения и роста пленок во многом определяет их кристаллическую структуру, а следовательно, и электрофизические, физико-химические, механические и эстетические свойства. Поскольку большинство ТП производства РЭА связано с осаждением или растворением пленок, необходимо рассмотреть физико-химические основы процессов зарождения и роста пленок новой фазы.
Пленки как элементы РЭА создаются на поверхности подложек при взаимодействии этих поверхностей с потоком частиц осаждаемых веществ. Результатом такого взаимодействия является появление новой фазы на поверхности подложки (пластины, детали, платы).
Потоки частиц могут иметь различный характер: молекулярные или ионные направленные пучки, потоки газовой и жидкой сред, движущиеся по законам газо- и гидродинамики, а также диффузионные потоки частиц. Процессы зарождения новой фазы могут протекать на границах различных фаз: жидкость — твердое тело, газ (пар) – твердое тело, твердое тело — твердое тело, композиционные пасты — твердое тело, жидкость — пар (газ).
Молекулярный пучок формируется, например, при испарении вещества. Этот пучок, достигая поверхности конденсации (подложки), имеющей температуру значительно ниже температуры испарения, конденсируется на ней, образуя пленку. Если температура конденсации (подложки) ниже температуры плавления вещества, то сначала образуются зародыши твердой фазы, а затем и сама твердая пленка. Если температура конденсации близка к температуре плавления вещества или выше ее, то формируется жидкая пленка. Однако в любом случае исходным материалом для создания пленки является поток частиц (молекул или атомов) от испарителя к подложке. Энергия этих частиц практически равна энергии испарения вещества.
В настоящее время существуют две теории гетерогенного образования зародышей конденсированной фазы: термодинамическая (макроскопическая) Гиббса — Фольмера и кинетическая (микроскопическая) Френкеля — Родина. Первая исходит из условий термодинамического равновесия в системе пар (газ) — зародыш — подложка, В ней используются такие термодинамические понятия, Как свободная и Поверхностная энергии, степень перенасыщения и др. Такой подход оправдан при небольших перенасыщениях пара, когда критический зародыш состоит из большого числа атомов, а следовательно, к нему применимы термодинамические законы. Однако во многих реальных процессах, когда степень перенасыщения велика (108 —1040 ), критический зародыш оказывается состоящим из одного атома. Описывать термодинамическими уравнениями столь малые агрегаты нельзя. В таком случае возможен лишь кинетический подход. Поэтому далее рассмотрены обе теории гетерогенного образования зародышей.
Если поток частиц J формируется за счет образования ионной плазмы при катодном или другом каком-либо способе распыления, то этот поток имеет сложный состав (включая нейтральные атомы, ионы и электроны в различных пропорциях). Так как энергии этих частиц могут отличаться друг от друга, то и характер их взаимодействия с поверхностью подложки будет различным, что скажется на механизме зарождения и роста пленок.
При химическом осаждении пленок (например, из газовой фазы) характер взаимодействия частиц с поверхностью еще более усложняется. Процесс протекает в несколько стадий:
1) адсорбция взаимодействующих молекул на этой поверхности;
2) диффузия молекул;
3) химическая реакция исходных компонентов с появлением молекул осаждаемого вещества;
4) адсорбция этих молекул и выделение их в отдельную фазу на поверхности;
5) десорбция летучих продуктов реакции. Аналогичная картина наблюдается и при электрохимическом осаждении пленок из электролитов.
При рассмотрении механизма зарождения и роста пленок будем исходить из двух предпосылок: наличия потока J вещества, направленного к поверхности осаждения, и теоретически чистой поверхности.
Процесс образования зародышей заключается в возникновении и росте агрегатов молекул в результате последовательных бимолекулярных реакций по схеме
где
![]() - агрегаты состоящие из i молекул (атомов),
- агрегаты состоящие из i молекул (атомов),
![]()
Агрегат, содержащий i=iкр молекул, рассматривается как зародыш критического размера, который в общем случае растет или уменьшается. Другие механизмы образования зародышей (например, одновременного столкновения iкр молекул или нескольких агрегатов размерами меньше критического) считаются вероятными только для потока, имеющего высокую плотность (например, для импульсных процессов испарения).
Образование сферического зародыша новой фазы, содержащего iкр молекул, сопровождается некоторым изменением свободной энергии ДGi , связанным с появлением определенной поверхности Sп и объема новой фазы V. В отсутствие полей и зарядов этот процесс можно описать уравнениями:
![]()
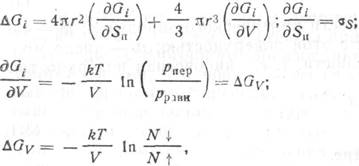
где r— радиус сферического зародыша, уS — поверхностная энергия, ДGV — изменение свободной энергии при конденсации, практически равное энергии испарения, рпер — давление перенасыщенного пара, рравн — равновесное давление пара, соответствующее температуре конденсации Т; N ↓ и N ↑— число молекул, движущихся к поверхности конденсации и испаряющихся с нее.
Следовательно, уравнение (3.2) можно представить в виде
![]()
![]()
![]()
![]() Зависимость ДGi
= f(r) для различных температур поверхности конденсации показана на рис. 3.1. Как видно из рисунка, свободная энергия ДGi
растет с увеличением rдо значения , а затем быстро убывает. Агрегаты радиусом r <rкр
считаются нестабильными, а радиусом r> rкр
— стабильными зародышами новой фазы. Последним соответствует уменьшение свободной энергии.
Зависимость ДGi
= f(r) для различных температур поверхности конденсации показана на рис. 3.1. Как видно из рисунка, свободная энергия ДGi
растет с увеличением rдо значения , а затем быстро убывает. Агрегаты радиусом r <rкр
считаются нестабильными, а радиусом r> rкр
— стабильными зародышами новой фазы. Последним соответствует уменьшение свободной энергии.
![]() Определив максимум функции (3.5) из условия , найдем радиус rкр
:
Определив максимум функции (3.5) из условия , найдем радиус rкр
:
![]()
Подставив значение rкр в (3.5),
![]()
![]()
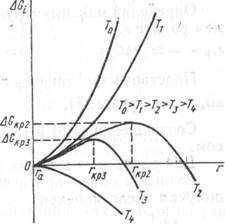
Соотношения (3.6) и (3.7) были впервые получены Дж. У. Гиббсом.
Для различных веществ rкр =1ч50 нм.
Разделив объем критического зародыша на молекулярный Vm , получим число молекул
![]()
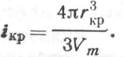
Из рис. 3.1 видно, что уравнение (3.5) справедливо в диапазоне температур от Т1 до Т4 . Вне этого диапазона теорию Гиббса — Фольмера использовать нельзя.
Скорость образования зародыша
![]()
![]()
где Sп.кр —площадь поверхности критического зародыша; щ — частота столкновений молекул с этой поверхностью; ni — число молекул на единице этой поверхности, т. е. равновесная поверхностная концентрация молекул.
По изотерме Вант-Гоффа
![]()
гдеn∑ — число молекул в паре.
Согласно уравнению Герца — Кнудсена частота столкновений
![]()
![]()
где ак — коэффициент конденсации; ри рк — давления насыщенных паров при температурах испарения и конденсации (т. е. испарителя и подложки). Следовательно, скорость образования зародышей
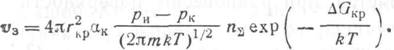
![]()
Уравнение (3.12) не учитывает ряда факторов. Например, не всякое столкновение молекулы с агрегатом ведет к ее конденсации и внедрению в агрегат. Поэтому выражение (3.12) следует умножить на равновесный фактор Z, учитывающий, какая доля из ударяющихся о поверхность молекул конденсируется. Обычно
![]()
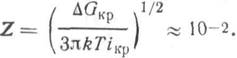
Таким образом,
![]()
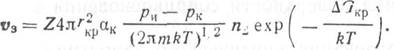
Все выкладки относятся к гомогенному образованию зародышей, которое редко реализуется на практике.
Модель гетерогенного образования зародышей отличается от гомогенной тем, что вводится геометрический фактор, определяемый межфазовыми взаимодействиями в системе подложка — зародыш— пар или подложка — зародыш — жидкость. Если свойства зародыша изотропны, то образуется куполообразный зародыш, если анизотропны —другие конфигурации зародышей (рис. 3.2).

Геометрический фактор вводится в уравнение (3.5) в виде функций поверхности соприкосновения зародыша с соответствующими фазами и объема зародыша fs (ц) и fv (ц), зависящих от контактного угла ц (для жидкостей — угла смачивания):

Эти функции описывают геометрическую конфигурацию зародыша. Значение ц определяется при равновесии поверхностных энергий:
Где упл-пар , ук-пр , ук-пар —удельные межфазовые поверхностные энергии поверхностей раздела пластина — пар, конденсат — пластина и конденсат —пар.
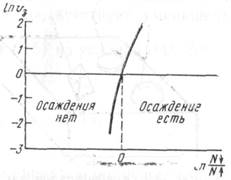


Для куполообразного зародыша
![]()
![]()
гдеfs пл (ц)—функция поверхности соприкосновения зародыша с пластиной; fs пар (ц) —функция поверхности соприкосновения зародыша с паровой фазой.
Свободную энергию образования критического зародыша найдем из условия максимума уравнения (3.15):
![]()
![]()
Где
![]()
![]()
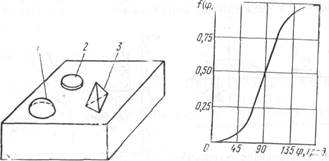
функция контактного угла f(ц) для куполообразного зародыша (рис. 3.3) характеризует взаимодействие конденсата с пластиной. При ц→0 f(ц)→0, ДGкр →0 и образование зародышей облегчается. При ц→1800 f(ц)→1, ДGкр растет до максимума и образование зародышей затрудняется (случай гомогенного зарождения новой фазы). Следовательно, уравнение (3.2) является предельным случаем образования зародышей, когда оно протекает с максимальной трудностью. Таким образом, свободная энергия гетерогенного меньше свободной энергии гомогенного образования зародышей. Кроме того, механизм гомогенного и гетерогенного образования зародышей (рис. 3.4) различен. При гомогенном образовании рост происходит только за счет реакции поверхности зародыша с паровой фазой (механизм х3 ), при гетерогенном — за счет поверхностной диффузии (механизм х2 ), т. е. х2 >>х3 . При очень низких температурах пластины х3 >х2 .
Скорость гомогенного образования зародышей в случае прямого осаждения из пара
![]()
![]()
где nадс — концентрация молекул, адсорбированных на поверхности; ДGк.п — свободная энергия конденсации из пара.
Скорость образования зародышей при преобладании поверхностной диффузии
![]()
![]()
где а — длина скачка диффундирующей молекулы к поверхности зародыша; j — величина, обратная числу возможных направлений скачков; v —частота поверхностных колебаний; ДGп.д — свободная энергия активации поверхностной диффузии; частота скачков диффундирующей молекулы.
![]()
При температурах пластины, позволяющих реализовать оба механизма образования зародышей, скорость образования зародышей равна сумме скоростей х2 и х3 :
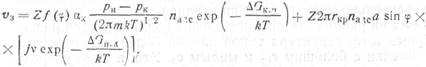
Для обычных условий осаждения пленок уравнение (3.22) удобно представить в виде
![]()
![]()
где К — константа, учитывающая размер критического зародыша и другие геометрические параметры; N —общее число частиц, участвующих в процессе образования зародышей.
Как видно из выражения (3.23), скорость образования зародышей существенно зависит от энергетических характеристик процесса, а следовательно, от условий осаждения. На рис. 3.5 показана логарифмическая зависимость скорости образования зародышей от скорости конденсации, характеризуемой степенью перенасыщения N↓/N↑.
Рост критических (докритических) зародышей за счет поверхностной диффузии возможен только в случае, когда температура пластины достаточно высока (kT>>ДGп.д ). При низких температурах диффузия атомов по поверхности мала и адсорбированные атомы можно считать локализованными. В этом случае рост зародыша происходит за счет прямого добавления атомов из пара (механизм х3 ). Скорость образования зародышей определяют по (3.20).
2. Влияние технологических факторов зарождения новой фазы на структуру пленок
Из уравнений (3.6) и (3.23) следует, что размеры критического зародыша rкр , его свободная энергия (энергетический барьер) ДGкр и скорость образования зародыша х3 зависят от значений поверхностной энергии, контактного угла, температуры, степени перенасыщения (скорости конденсации), энергии активации поверхностной диффузии. Эти характеристики могут рассматриваться как технологические параметры ТП и исходных материалов, поэтому проанализируем их влияние на стадии образования зародышей и формирования первых (моноатомных) слоев.
Пленка, образованная при высоком энергетическом барьере, должна состоять из зародышей, имеющих большой критический радиус и низкую скорость зарождения (малое число зародышей), т. е. состоять из нескольких крупных агрегатов. Пленка, образованная при низком энергетическом барьере, должна состоять из зародышей, имеющих малый критический радиус и высокую скорость зарождения (большое число зародышей), т. е. состоять из большого числа мелких агрегатов. Такая пленка становится сплошной при относительно малом значении средней толщины, поскольку зародыши уже на ранних стадиях осаждения соприкасаются и срастаются. Кроме того, структура такой пленки более мелкодисперсная, чем у пленки с большим rкр и малым х3 . Это, в свою очередь, будет сказываться на электрических свойствах полученных слоев. Таким образом, анализ влияния технологических параметров на rкр , ДGкр , х3 может в первом приближении дать ответ на характер их взаимной зависимости и связь с электронными свойствами полученных слоев.
Сопоставление приведенных данных указывает на существенную зависимость rкр от природы осаждаемого материала и особенно от такого его свойства, как давление насыщенного пара, связанного с теплотой испарения. Поскольку теплота испарения прямо пропорциональна точке кипения (согласно правилу Трутона), можно заключить, что материалы с высокой температурой кипения обладают большим значением ДGV . Следовательно, размеры критических зародышей должны уменьшаться с повышением температуры кипения вещества пленки. Поэтому у металлов с высокой температурой кипения (W, Мо, R е, Та, Ni, Cr и др.) даже очень малые зародыши являются стабильными. У металлов с невысокой температурой кипения (Zn, Cd, Ag, Au, Cu и др.) зародыши должны достичь значительной величины, прежде чем стать стабильными. С увеличением размеров их устойчивость повышается.
При срастании агрегатов между ними формируются границы зерен. Таким образом, размер зерен образующейся пленки определяется величиной критических и (сверхкритических) зародышей. В свою очередь, как подчеркивалось ранее, структура пленки влияет на ее электрофизические свойства. Окончательные размеры зерен зависят и от режимов последующей обработки пленки, например ее отжига при определенных температуре, времени, давлении и т. п. Исследования тонких пленок показали, что материалы пластины и испаряемого вещества, а также условия осаждения влияют на структуру пленок.
Из приведенных соотношений следует, что размеры критических зародышей резко снижаются, если материал пластины имеет большое сродство с осаждаемым веществом, т. е. малый угол ц. Например, если в качестве материала пластины служит металл, для которого уS = 1,5 Дж/м2 , ц→0, то при осаждении алюминия rкр может иметь значение, близкое к нулю, что указывает на отсутствие энергетического барьера при зарождении пленки даже у металлов с высоким давлением насыщенного пара. Поэтому образование сплошных пленок может происходить при нанесении на металлическую или полупроводниковую пластину даже нескольких моноатомных слоев осаждаемого металла. Такое явление часто используется в технологии РЭА для создания адгезионных подслоев при получении пленок из материалов, имеющих малое сродство с пластиной (плохую адгезию к пластине). При этом сначала на пластину напыляют какой-либо материал с малым рк и хорошей адгезией к пластине (ц→0), например Сr или W, затем на него — основной металл (А1, Сu, Аu и т. п.), который будет осуществлять ту или иную заданную электрическую функцию.
Влияние температуры пластины на размеры критического зародыша определяется зависимостью, полученной в результате дифференцирования выражения (3.6) по температуре:
![]()
![]()
Согласно средним значениям величин, входящих в (3.24) для металлов, уS = 1 Дж/м2 , ∂ДGv /∂T≈ДSисп ≈8,8∙106 Дж/(м3 ∙К); дуS /дТ≈5∙10-4 Дж/(м2 ∙К) при | ДGv | <1,64∙1010 Дж/м3 получим
![]()
![]()
что имеет место практически во всех случаях, когда существует энергетический барьер образования зародышей.
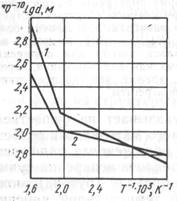

Следовательно, увеличение температуры пластины ведет к росту rкр и сохранению островковой структуры и для более высоких значений средней толщины пленки. На рис. 3.6 приведена зависимость среднего расстояния dмежду агрегатами (плотности агрегатов) от температуры пластины при термическом испарении и катодном распылении. Угол наклона кривых 1 и 2 позволяет определить ДGп.д.
Продифференцировав ДGкр по температуре, найдем
![]()
![]()
Поскольку скорость образования зародышей х3 экспоненциально связана с ДGкр [см. уравнение (3.23)], скорость возникновения агрегатов критических и сверхкритических размеров быстро убывает с ростом температуры. В этом случае для создания сплошной пленки потребуется более продолжительное время.
Влияние скорости осаждения пленки (степени перенасыщения) на размеры критических зародышей (rкр ) и ДGкр обусловлено зависимостью этой скорости от значения ДGv [см. (3.3) и (3.4)]. При увеличении N↓ или рпер (ри —pк ) возрастает ДGv . Поскольку поверхностные энергии пластины и границы раздела не зависят от N↓,
![]()
![]()
Следовательно, рост скорости осаждения пленки приводит к уменьшению размеров зародышей и увеличению скорости их возникновения. Поскольку зависимость ДGv = f (N↓) является логарифмической, влияние скорости осаждения пленки на значения rкр и ДGкр сказывается очень сильно.
Повышение скорости осаждения при реальных условиях может привести и к увеличению размеров критических зародышей, т. е. зависимость rкр = f(N↓) является более сложной, чем описываемая теорией Гиббса — Фольмера.
Влияние поверхностной диффузии на размеры критического зародыша аналитически определить нельзя. Однако скорость образования критических зародышей должна зависеть от способности адсорбированных атомов диффундировать и сталкиваться друг с другом. Согласно уравнению (3.23) эта скорость уменьшается экспоненциально с увеличением энергии активации поверхностной диффузии. Если энергия активации велика, то диффузия протекает медленно и зародыши растут только за счет столкновения их с атомами паровой фазы. Энергию активации диффузии часто принимают равной 1/4 энергии активации десорбции в газовую фазу, т. е.
![]()
Энергия связи осаждаемых атомов с пластиной ДGадс , как показано ранее, влияет на значения rкр и ДGкр . Поэтому для неоднородных поверхностей пластин, где ДGадс заметно изменяется от участка к участку, на различных участках пластины значения rкр и ДGкр различны, что сказывается на однородности осаждаемой пленки. Вот почему в технологии РЭА необходимо иметь подложки с однородной и чистой поверхностью.
Энергия адсорбции для некоторых металлов имеет следующие значения:
![]()
3. Рост пленок. Эпитаксия
В радиоэлектронике используются пленки, реальная толщина которых во многих случаях больше, чем высота купола критических и сверхкритических зародышей. Поэтому необходимо рассмотреть не только образование, но и развитие (рост) пленки после того, как она стала сплошной, т. е. после исчезновения островковой структуры. При этом следует определить:
1) степень влияния механизма образования зародышей на дальнейшую структуру пленки, а также на возникновение границ зерен, дефектов структуры: упаковки, двойниковых структур, вакансий, дислокаций и др.;
2) зависимость изменения или повторения образовавшейся структуры от механизма роста пленок и различных параметров состояния;
3) способы влияния на изменение структуры пленки с целью улучшения ее электрофизических свойств.
Осаждение монокристаллических пленок на монокристаллические пластины называют эпитаксией. В понимании механизма роста пленок эпитаксия играет большую роль.
Эпитаксиальная пленка когерентна со структурой пластины, т. с. повторяет эту структуру. Такая пленка может «наследовать» или «залечивать» дефекты пластины в зависимости от условий осаждения и ее обработки.
После того как получен первый сплошной слой пленки, следующий слой формируется независимо от структуры пластины. Рост отдельного агрегата на атомарном уровне может быть как эпитаксиальным, так и неэпитаксиальным. Для анализа механизма роста пленки воспользуемся моделью образования куполообразного зародыша, описанной в п.1.
Согласно уравнению (3.18) свободная энергия образования критического зародыша
![]()
При осаждении пленки на предыдущий слой того же материала можно принять ц = 0. Тогда f(ц) =0 и ДGкр = 0. Следовательно, энергетический барьер отсутствует. Поэтому конденсирующиеся атомы на поверхности пленки непосредственно встраиваются в структуру растущего слоя. В этом случае классическая модель образования зародышей макроскопических размеров не применима к образованию микроскопических (например, двухатомных или трехатомных) агрегатов. После возникновения на пластине сплошной пленки ее рост следует рассматривать с позиций роста кристаллов. Поверхность кристалла никогда не бывает идеально гладкой. На ней всегда имеются различные выступы, ямки, островки и другие неоднородности структуры (рис. 3.7). Механизм роста пленки включает в себя адсорбцию атомов из паровой фазы (преимущественно на гранях кристалла), поверхностную диффузию к ступеньке, взаимодействие со ступенькой, диффузию вдоль ступеньки и достраивание ступеньки. В зависимости от того, какое положение занимает адсорбированный атом на поверхности кристалла, число атомов, окружающих его, различно. Поэтому различна и энергия связи его с поверхностью кристалла, а следовательно, и энергия активации поверхностной диффузии.
Условия равновесия, которые существуют между различными положениями атомов (рис. 3.7), таковы:
![]()
![]()
где пi 1 , пi 2 , пi 3 , пi 4 — равновесные концентрации атомов соответствующего типа; рМе —давление пара осаждаемого компонента; х1 , х2 ,…, х10 — скорости движения атомов.
Скорости х5 — х10 , влияющие на рост пленки, можно найти следующим образом:
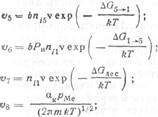
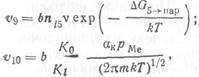
где b - длина ступеньки на единицу площади; v≈1013 с-1 —частота колебаний атомов, находящихся на поверхности пленки; ДG1→5 , ДG5→1 — свободные энергии диффузии атомов при переходе из положения 1 в положение 5 и обратно; Рн — вероятность данного направления движения атомов при их миграции по поверхности пленки (для плотно упакованных кристаллов Рн =1/6); Ко , Ki — число позиций атомов на единичной поверхности и длине ступеньки.
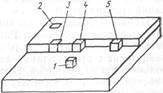

Таким образом, анализ роста пленки сводится к выявлению преобладающей стадии роста в тех или иных задаваемых условиях. Для случая, когда преобладает скорость поверхностной диффузии х6 , а скоростью диффузии вдоль ступеньки х4 можно пренебречь, уравнение диффузии для адсорбированных атомов примет вид
![]()
![]()
Где DS — коэффициент поверхностной диффузии; х — координата движения частицы.
Выражение (3.30) является кинетическим уравнением роста пленок.
Анализ роста монокристаллических (эпитаксиальных) пленок позволяет выявить кроме первичных дефектов структуры, вызванных условиями зарождения, и вторичные дефекты, появляющиеся в процессе роста,— дислокационные петли, дефекты упаковки и точечные дефекты. Часто встречающимися дефектами в пленках являются дислокации. Концентрация дефектов условно характеризуется плотностьюдислокации, измеряемой их числом на 1 см2 . Эта величина в эпитаксиальных пленках металлов достигает нередко значений 1010 —1011 см-2 . В полупроводниковых эпитаксиальных пленках, используемых в производстве ИМС, плотность дислокаций составляет 10—104 см-2 .
Причины появления дислокаций различны. Пленки формируются в процессе осаждения. Ранее осажденные слои могут покрываться последующими до того, как будет достигнуто термическое равновесие с предыдущим слоем. При этом в слой может попадать большое число вакансий. Процесс усугубляется, если температура пластин низкая. В этом случае тепловой энергии (конденсации) может не хватить для того, чтобы обеспечить миграцию атомов по поверхности. Поэтому атомы будут оставаться в тех местах, куда они попали при соударении с поверхностью. Поскольку их распределение носит случайный характер, они будут вносить разупорядоченность в структуру осаждаемой пленки. Степень разупорядоченности зависит от наличия примесей в пленке и на ее поверхности, а также от неоднородных поверхностных свойств предыдущего слоя, низкой температуры конденсации и т. п.
4. Химический рост эпитаксиальных пленок
В предыдущих параграфах были рассмотрены процессы образования и роста пленок при испарении и конденсации согласно термодинамической теории Гиббса — Фольмера, справедливой для степени перенасыщения, не превышающей 108 . При испарении тугоплавких металлов (W, Mo, Re, V) степень перенасыщения достигает значений 1030 —1040 ; размеры критических зародышей, рассчитанные по уравнению (3.6), соответствуют размерам одного атома и меньше, что противоречит физическому смыслу. Аналогичная ситуация возникает и при осаждении слоев химическими способами из газовой фазы, где степень перенасыщения составляет 1020 —1040 . В этом случае единственно приемлемой теорией для анализа роста пленок является кинетическая теория Френкеля — Родина.
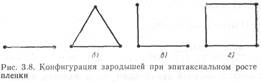
Пока не существует достаточно разработанной теории образования и роста эпитаксиальных слоев. Излагаемая теория Френкеля— Родина устанавливает лишь ряд важных закономерностей, часто подтверждаемых экспериментально.
В1924 г. советский ученый Я. И. Френкель ввел понятие двумерного пара (газа). В соответствии с этим понятием атомы, попавшие на поверхность твердого тела из объема паровой или газовой фазы, адсорбируются этой поверхностью и удерживаются на ней в течение времени:
![]()
![]()
где ф0 = 10-13 с —время, соответствующее дебаевской частоте; ДGадс — свободная энергия адсорбции атома; Т — температура поверхности.
Частицы двумерного пара, мигрируя по поверхности, сталкиваются друг с другом, образуя агрегаты из двух, трех и т. д. атомов. Простейшим агрегатом является двойник (i = 2), показанный на рис. 3.8, a, с энергией межатомной связи Е11 и энергией связи с поверхностью 2E12 . Поскольку двухатомные агрегаты вдвое сильнее связаны с поверхностью, чем одиночные атомы, они и менее подвижны. Для испарения двойника нужна энергия 2E12 , а одного атома Е12 . При осаждении металлов и полупроводников на диэлектрические пластины Е11 >Е12 ; процесс испарения двойника менее вероятен, чем одного атома, что соответствует образованию зародыша конденсированной фазы. При увеличении агрегата (i= 3, 4,..., п) вероятность образования зародышей увеличивается.
При очень большом перенасыщении газовой фазы критический зародыш может состоять из одного атома. Поэтому, когда возникает агрегат из двух атомов, более вероятно, что он будет расти, а. не распадаться. Снижение перенасыщения приводит к тому, что вероятность присоединения к одному атому другого становится равна вероятности распада агрегата. В таком случае стабильными станут конфигурации с двумя связями на атом. При дальнейшем, снижении перенасыщения стабильными становятся агрегаты из трех, четырех и т. д. атомов (рис. 3.8, а—г). Стабильными образованиями являются треугольник и квадрат. В первом случае зародыш имеет ориентацию <111>, во втором — <100>. Таким образом, степень перенасыщения должна сказываться на ориентации стабильных зародышей.
Зависимость скорости хK образования зародышей (конденсации) из потока I частиц, попадающих на пластину, от температуры пластины Т может быть описана следующими уравнениями:
![]()
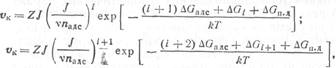
где падс — число единичных адсорбированных атомов; v — частота колебания адсорбированного атома; ДGi , ДGi +1 — свободные энергии образования зародыша в результате межатомного взаимодействия (аналог ДGк.п при эпитаксии).
Поскольку iневелико, можно методом проб и ошибок установить, какое значение i(1, 2, 3,...) отвечает экспериментальным данным.
Процессы образования эпитаксиальных слоев во многом определяют характер их роста и, следовательно, степень кристаллического совершенства полученной структуры. При значительной разориентации отдельных зародышей слой будет иметь большое число дефектов и может стать неприемлемым для изготовления ИМС.
Наибольшее распространение в промышленной практике получили процессы эпитаксии полупроводников из газовой фазы с помощью химических реакций.
Развитие методов эпитаксии, особенно гетероэпитаксии (выращивания пленки одного материала на подложке другого), позволяет получать приборы с такими высокими электрическими характеристиками, которые трудно реализовать другими технологическими методами.
Глава 2. Физико-химические основы поверхностных процессов
1. Термодинамика поверхностных процессов
Свойства поверхности раздела отдельных слоев структуры или конструкции функциональных узлов, состоящих из металлов, диэлектриков, полупроводников, композиционных материалов, важны при формировании практически всех элементов и компонентов РЭА. Они зависят от сложных комплексных характеристик поверхностей раздела на атомарном и субатомарном уровнях, а также взаимодействия этих поверхностей с полями (электрическими, электромагнитными) и излучениями (электромагнитными, оптическими, атомными и субатомными). Изменение характеристик поверхности раздела под действием внешних и внутренних факторов приводит к необратимым изменениям параметров качества изделий РЭА. Характеристики поверхностных и приповерхностных слоев влияют на все эксплуатационные параметры РЭА.
Знания физико-химических свойств поверхностей твердых тел хотя и расширились в последнее десятилетие, однако еще недостаточны для установления количественных взаимосвязей параметров качества изделий и технологических факторов. Эти взаимосвязи важны для выбора оптимальных технологических решений при обработке, эксплуатации и сохранения свойств поверхностных и приповерхностных слоев в РЭА.
Любое технологическое воздействие среды на материал или изделие, как правило, начинается с взаимодействия частиц этой среды с поверхностью материала (изделия). Для большинства ТП производства РЭА необходимо знать механизм такого взаимодействия не только при формировании (зарождении, росте, травлении), но и при эксплуатации слоев. Это требует от технологов тщательного изучения явлений и процессов, которые могут протекать на поверхности при различных условиях (технологических факторах).
Термодинамика поверхностных явлений рассматривает состояния поверхностных атомов, отличающихся от состояния атомов, расположенных во внутренних слоях вещества. Причиной этого различия является неодинаковое взаимодействие атомов твердого тела с окружающими частицами. Поэтому свойства поверхностного слоя вещества отличаются от свойств его внутренних слоев. Следовательно, необходимо различать поверхностные и объемные свойства вещества. Чем больше отношение площади поверхности твердого тела к его объему, тем сильнее сказывается влияние поверхностных свойств на общие. Поверхностные свойства веществ проявляются на любой поверхности раздела фаз: твердое тело — газ, твердое тело — твердое тело, жидкость — пар, жидкость — жидкость.
Термодинамические параметры поверхности определяются природой материала и его физическим состоянием, которое характеризуется полной поверхностной энергией. Часть этой энергии, равная максимальной полезной работе, затрачиваемой на создание поверхности, является удельной поверхностной энергией Гиббса и называется поверхностным натяжением уS .
Значения поверхностного натяжения для жидких материалов определить экспериментально легко (представлены в справочниках), а для твердых — трудно.
Для большинства расчетов уS для твердых тел принимаются на 5—8% больше этих же значений для жидких.
Идеальная (чистая) поверхность встречается редко. На практике приходится иметь дело с реальной поверхностью, т. е. поверхностью твердого тела, покрытой пленкой (толщиной 100—1000 нм) оксидов, гидратов, жиров и других веществ, которая к тому же не является атомно гладкой, В микроэлектронных изделиях большинство эксплуатационных свойств реализуется в приповерхностных слоях. Состояние поверхности влияет на электрофизические параметры приповерхностных слоев, вызывая адсорбцию заряженных частиц, появление рекомбинационных центров и других дефектов. Часто надежная работа радиоэлектронного устройства зависит от того, насколько хорошо подготовлена (обработана) и насколько надежно защищена его поверхность от вредных внешних воздействий. Для того чтобы понять физико-химические свойства поверхности, рассмотрим основные термодинамические и физические аспекты поверхностных явлений.
Поверхностное натяжение уS влияет на значение суммарной свободной энергии системы ДG только в том случае, когда оно соизмеримо с другими составляющими уравнения. При термодинамическом анализе поверхностных явлений определяются значимость уS в уравнении, возможности еенахождения, зависимость уS от таких параметров состояния, как температура, давление, концентрация компонентов системы, или от технологических факторов (чистоты, шероховатости поверхности и т. п.).
При повышении температуры происходит расширение тел и ослабление сил взаимного притяжения как в толще, так и на поверхности материала. Это приводит к тому, что поверхностное натяжение уменьшается с увеличением температуры материала. Зависимость поверхностного натяжения от температуры в большинстве случаев линейна.
В этих условиях поверхности раздела фаз не существует. В конденсированном состоянии (жидком или твердом) вещество не может находиться выше температуры Ткр . Такую температуру называют критической. На практике часто пользуются этим параметром, например, для полного удаления влаги из какого-либо технологического агрегата или с поверхности изделий производят их термическую обработку при температуре, близкой к критической температуре воды (475°С). В большинстве случаев достаточной является температура 300°С, особенно если сушка проводится в вакууме.
При постоянных температуре и давлении самопроизвольно протекают такие процессы, для которых характерно уменьшение свободной энергии, т. е. ДGS <0 или ДG3 = уS ДSп <0. Если уS =const, то ДSп <0, т. е. протекающие процессы сопровождаются уменьшением площади поверхности. Таким образом, система самопроизвольно стремится к уменьшению поверхности раздела фаз.
Для жидкости поверхностное натяжение уS минимально при шарообразной форме. Для кристаллических тел наименьшее значение ДGS достигается при определенных соотношениях размеров граней кристалла, поскольку поверхностные энергии различных граней различны. Конфигурация кристалла, которой соответствует минимум ДGS , наиболее устойчива (принцип Гиббса — Кюри).
Важным выводом термодинамического анализа поверхностных процессов является то, что при увеличении площади поверхности, т. е. при повышении дисперсности (степени измельчения) вещества, его пористости, разрыхленное™ внутренней структуры и степени ее упорядоченности, изменяются физико-химические и эксплуатационные свойства материалов, а следовательно, и изделий, изготовленных из них. Например, у мелкодисперсных материалов увеличивается способность к переходу из одной фазы в другую при любом процессе (увеличиваются летучесть, растворимость, химическая активность и т. п.). Материал более активен в аморфном состоянии, чем в кристаллическом; в поликристаллическом, чем в монокристаллическом. На практике это свойство материалов используется широко, например, для эмульсий галогенидов серебра, применяемых в фотолитографии, степень дисперсности определяет светочувствительность материала; при создании изделий из композиционных паст энергия сцепления частиц в значительной мере зависит от степени их дисперсности и т. п.
При взаимодействии поверхностей твердой и жидкой фаз наблюдается явление, называемое смачиванием. Степень смачивания характеризуется видом и степенью искривления поверхности жидкости в месте соприкосновения трех фаз: твердой, жидкой, паровой (газообразной). Такое искривление называют мениском.
Степень смачивания определяет форму капли жидкости на стенки сосуда твердой поверхности. Мерой смачивания обычно служит контактный угол (угол смачивания) ср между смачиваемой поверхностью и поверхностью жидкости по периметру смачивания (рис. 4.1, а).
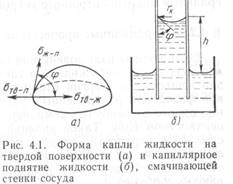
Если соприкасаются две поверхности твердого тела, т. е. судить о смачивании невозможно, то вводится аналогичное смачиванию понятие адгезии как явления и меры взаимодействия двух (более) поверхностей твердых тел. Адгезия измеряется силой отрыва одной поверхности от другой.
Смачивание, адгезия и капиллярные явления играют существенную роль при промывке и сушке изделий и полуфабрикатов (замедляют движение жидкостей и газов из пор и трещин), а также в пропитке, осаждении слоев, лужении, пайке и сварке изделий. Кроме того, эти явления могут влиять на эксплуатационную надежность таких многослойных тонкопленочных изделий, как интегральные микроэлектронные устройства.
2. Адсорбционные процессы на поверхности твердых тел
Если энергия взаимодействия поверхностей двух конденсированных фаз (например, жидкой и твердой) определяется силами адгезии веществ, то энергия взаимодействия поверхности тела с газовой фазой или разбавленным раствором вызывает концентрирование одного из веществ (компонентов) на поверхности и в приповерхностном слое. Такое явление называется адсорбцией. Вещество, на поверхности которого происходит адсорбция, называется адсорбентом, а адсорбируемое вещество — адсорбагом. Процесс отделения от поверхности ранее адсорбированного вещества называют десорбцией.
Различают два вида адсорбции: физическую и химическую (хемосорбцию). При физической адсорбции энергия взаимодействия между адсорбатом и поверхностью не столь значительна, чтобы изменить физико-химическую природу адсорбата, а следовательно, и его свойства. При хемосорбции образуется химическая связь между поверхностью и адсорбируемым веществом.
Физическая адсорбция протекает быстро, особенно при понижении температуры поверхности. Хемосорбция при низких температурах протекает медленно, но при повышении температуры ее скорость быстро растет подобно скорости химических реакций. Энергия физической адсорбции соизмерима с теплотой конденсации (испарения). Для органических растворителей она составляет 8— 15 кДж/моль, для металлов —10—40 кДж/моль. Энергия хемосорбции сравнима с теплотой химических реакций (50— 400 кДж/моль).
Количественную характеристику адсорбции можно получить из уравнения
![]()
![]()
где GG — свободная энергия Гиббса; S — энтропия системы; k— число компонентов системы; мi — химический потенциал i-ro компонента; Сi — концентрация i-ro компонента.
При Т = const, p = const в условиях равновесия (dGg = 0)
![]()
![]()
Адгезия различных пленок к подложкам позволяет обеспечивать получение качественных и надежных функциональных устройств, пассивирующих слоев и декоративных покрытий РЭА. Поэтому необходимо проанализировать факторы, стимулирующие и подавляющие адгезию. Решать эту проблему без учета природы конкретных материалов подложки и пленки не представляется возможным, так как характер взаимодействия адгезируемых материалов зависит не только от параметров состояния (температуры, состава, давления), но и от природы взаимодействующих веществ.
Пограничные слои пленки и подложки могут образовывать и химические связи, которые практически не поддаются расчету, а могут лишь качественно оцениваться исходя из химических свойств взаимодействующих поверхностей. Ориентиром в таких оценках может служить сродство осаждаемого (наносимого) на поверхность подложки вещества пленки к веществу подложки или какому-либо компоненту этого вещества. Например, при осаждении металлической пленки на поверхность подложки, изготовленной из оксидов тех или иных элементов (Si02 , A12 03 , Zr02 ) или их композиций, важным фактором для адгезии является сродство осаждаемого металла к кислороду и возможность образования химических (типа химических) связей Me—О. Очевидно, что адгезия пленки при возникновении химической связи на границе раздела значительно больше, чем при чисто физической связи. Если при физической адгезии энергия отрыва пленки от подложки приблизительно равна теплоте сублимации, то при химической адгезии (хемоадгезии) эта энергия должна быть соизмерима с энергией диссоциации связи Me—О, которая, как правило, на порядок больше теплоты сублимации (сотни, десятки кДж/моль). Таким образом, при прочих равных условиях металл, имеющий большее сродство к кислороду, имеет лучшую адгезию к материалу из оксидов, причем повышение температуры в этом случае увеличивает адгезию в отличие от физической адгезии, при которой повышение температуры приводит к уменьшению силы адгезии.


Сила адгезии по всей поверхности подложки одинакова, если поверхность однородна, т. е. ее рельеф и чистота постоянны. На молекулярном (атомном) уровне практически любая поверхность неоднородна. На практике используют различные эмпирические критерии однородности и чистоты поверхности, пригодные для оценки технологии ее обработки.
Шероховатость (степень неоднородности рельефа) поверхности влияет на силу адгезии. Можно привести множество примеров адгезии частиц пленки на неоднородных поверхностях (рис. 4.8, а, б) и только один пример на идеально гладкой поверхности (рис.4.8, в). Поэтому понятно стремление технологов добиться как можно более гладких поверхностей для обеспечения максимальной адгезии.
Такой же вывод можно сделать и относительно чистоты поверхности. Из анализа рис. 4.8 можно понять, как могут зарождаться и исчезать поры, трещины и другие «слабые» места на границе раздела пленок и подложек. При малых размерах частицы пленки могут «грунтовать» поверхность, обеспечивая хорошую адгезию последующих слоев. Для получения хорошей адгезии слабо адгезирующего материала промежуточные слои формируют из веществ, имеющих хорошую адгезию к подложке и материалу пленки. Такие вещества, обеспечивающие высокую адгезию, называют адгезивами.
Для оценки шероховатости поверхности используют классы чистоты (обработки) поверхности. В табл. 4.1 приведены параметры, характеризующие шероховатость поверхности (см. рис. 4.8, а).
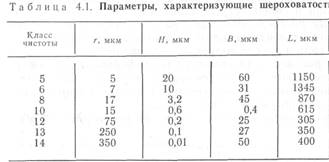 |
Физическая (пыль, вода, жиры) и химическая (оксиды, карбиды, нитриды) чистота поверхности могут влиять на адгезию вещества как в положительную (увеличения), так и отрицательную (уменьшения) сторону в зависимости от физико-химических свойств загрязняющего материала. В большинстве случаев пыль, вода и жиры, создавая неровности и поры на границе раздела пленки и подложки, снижают адгезию пленки. Если осаждаемая пленка лучше адгезирует с оксидами (нитридами, карбидами и т. п.), то такие загрязнения способствуют увеличению адгезии. Загрязнения поверхности могут рассматриваться с физико-химической точки зрения как источник промежуточных сил, по-разному влияющих на адгезию пленок и покрытий. В любом случае физико-химическая неоднородность поверхности приводит к нестабильным значениям адгезии.
4. Процессы очистки, промывки и пропитки поверхности
При нанесении различных жидких материалов на поверхность твердых тел происходит их смачивание, определяемое силами сцепления жидкости и поверхности твердого тела. Хорошее смачивание необходимо в процессах, в которых осуществляется взаимодействие жидкой среды с поверхностью (нанесение фотоэмульсий, жидких красителей, травление, лужение, панка, очистка химическими растворителями, пропитка и т. п.).
Стабильные результаты при смачивании поверхности жидкостью можно получить только при наличии достаточно чистой поверхности твердого тела. Поэтому тщательная очистка поверхности жидкими растворами характерна для ТП, связанных с нанесением пленок или паст (нанесение покрытий, пропитка, осаждение пленок и т. п.).
Основные виды загрязнения поверхности (жиры, пыль, припои, оксиды, соли) можно удалить с помощью жидких растворителей. Для интенсификации процессов растворения применяются гидродинамическая (отмывка щетками и сильной струей растворителя) и гидроакустическая (отмывка с помощью акустических волн, распространяющихся в растворителе) обработки.
По своей физико-химической природе растворители делятся на неорганические (вода, соли, кислоты, щелочи), органические (ацетон, четыреххлористый углерод, бензин и др.), смешанные (спиртовые растворы, водные растворы органических кислот), а также расплавы металлов и солей (ртуть, олово, галлий, припои и др.). Неорганические растворители, как правило, гидрофильны. По своей природе они относятся к классу электролитов, хорошо растворяют оксиды, соли и другие полярные соединения.
Органические растворители являются гидрофобными и относятся к классу неэлектролитов. Они хорошо растворяют примеси органического происхождения (неполярные или слабополярные вещества), например жиры, минеральные масла.
Смешанные растворители состоят из смесей растворителей обоих типов.
Расплавы металлов и солей используются как растворители при повышенных температурах ТП.
Пока еще не известен растворитель, который мог бы очищать поверхность от всех загрязнений. Поэтому используются многостадийные методы очистки поверхностей в растворах разного типа. Очистка растворителями интенсифицируется с помощью нагрева или применения ультразвука. При нагревании снижаются вязкость и поверхностное натяжение растворителя, что облегчает проникновение его в зазоры и поры для удаления загрязнений. Те же функции выполняет ультразвук частотой 40—700 кГц.
Перемешивание растворителя увеличивает массопередачу растворенного вещества от поверхности в глубь раствора, обеспечивая приток раствора, менее загрязненного примесью, к поверхности.
В табл. 4.2 приведены физико-химические свойства основных растворителей, используемых для очистки поверхностен изделий, а в табл. 4.3 дан перечень растворяемых в них загрязняющих веществ.
На обрабатываемых поверхностях деталей присутствуют жиры и минеральные масла, нерастворимые в воде. Удалить их с поверхности можно лишь органическими растворителями или щелочными растворами. Под действием щелочи жиры омыляются, образуя растворимые в воде соли жирных кислот (мыла) и глицерин, согласно взаимодействию стеарина с едким натром.
Для удаления загрязнений могут использоваться различные механические и гидродинамические приспособления: щетки, полотна, сильные водяные струи и т. п.
При подготовке поверхностей деталей или узлов к нанесению жидких эмульсий (смачивание), пропитке с целью герметизации и изоляции и т. п. необходимо обеспечить максимальную адгезию этих материалов с подложкой. Тщательная очистка поверхности недостаточна для обеспечения надежной адгезии. Следует повысить и физико-химическую активность поверхности, что достигается ее химическим травлением. Травитель должен очищать поверхность, удаляя с нее вредные для дальнейших ТП вещества.
Большинство изделий и деталей РЭА выполняется из различных веществ или материалов. Поэтому травильные растворы имеют селективный характер, т. е. способны растворить один материал, не затрагивая другие. Составы травителей подбираются экспериментально в зависимости от свойств поверхности, которые необходимо получить, заданной скорости травления, удобства работы с травителем и его хранения, токсичности, горючести, стоимости и т. п.
Хорошие адгезионные свойства поверхности позволяют обеспечить высокое качество ТП пропитки изделий РЭА. Целью пропитки как ТП производства РЭЛ является увеличение влаго- и термостойкости изделий, а также улучшение их механических и электрических свойств (ликвидация вибраций в катушках индуктивности и трансформаторах, снижение токов утечки, исключение явлений ионизации, улучшение теплоотвода и т. п.).
При пропитке пропитывающий материал должен проникнуть во все щели, вытесняя из них воздух, и хорошо смочить обрабатываемую поверхность. Это возможно только при достаточно высокой адгезии материала с поверхностью обрабатываемого изделия или детали, т. е. при малой вязкости пропитывающего материала; достаточно чистой поверхности обработки и удалении воздуха из щелей за счет разрежения.
Это обеспечивается выбором маловязких пропитывающих жидкостей и их нагреванием непосредственно перед пропиткой; тщательной очисткой и травлением поверхностей описанными методами; применением вакуумной пропитки или пропитки под давлением.

Пропитка, как и любое другое покрытие поверхностей, осуществляется в несколько стадий. При этом образуется многослойная покрывающая структура, предохраняющая поверхность от воздействия различных внешних факторов за счет несовпадения рельефа трещин и порв соприкасающихся слоях (рис. 4.11).
Хемоадгезия по аналогии с хемосорбцией повышает адгезию покрытия за счет образования химических связей, особенно сильно проявляющихся при наличии на поверхности и в покрытии гидроксильных или фенольных групп (рис. 4.12).
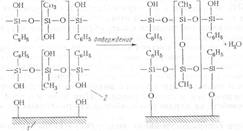

Часто для снижения вязкости пропитывающие термореактивные смолы разбавляют растворителями, которые затем удаляются при отверждении . Однако удаление растворителей при отверждении может привести к появлению новых пор и трещин. Кроме того, большинство растворителей являются химически активными веществами, способными растворять материалы конструктивных элементов изделия (эмали обмоточных проводов, пленки и т. п.). Поэтому с физико-химической и технологической точек зрения лучше подбирать такие составы для пропитки, которые можно использовать без растворителей, например на основе эпоксидных полиэфирных и полиуретановых смол.
Если требуется получить малую вязкость пропитывающего материала при низких температурах, следует использовать полиэфирные смолы. Достоинствами таких смол являются их доступность и низкая стоимость. Если необходима высокая эластичность пропитывающего материала после отверждения, то нужно применять полиуретановые смолы.
В пропитывающие составы обычно вводятся смесительные отвердители, ускоряющие процесс отверждения и упрочняющие эти составы. Кроме того, такие смеси могут использоваться для заливки изделий. В качестве отвердителей применяются полиангидриды типа полиазилена.
Смешивая пропитывающие вещества различных составов и смолы, можно получить имеющие широкий диапазон твердости материалы. Для пропитки деталей и узлов СВЧ-аппаратуры выпускаются специальные составы с малыми потерями и вязкостью от 0,01до 20 Па∙с.
Таким образом, основными параметрами, определяющими качественное протекание процессов пропитки и заливки, являются:
— температура и давление процесса, степень чистоты и структура поверхности, обеспечивающие наилучшее взаимодействие поверхности с пропитывающим (заливочным) материалом;
— температура, состав, вязкость, электрофизические и механические свойства пропитывающего (заливочного) материала;
— скорость пропитки (заливки), т. е. скорость затвердевания (отверждения) пропитывающих составов и особенно деградация эксплуатационных характеристик этих материалов по границам раздела (взаимодействующим поверхностям) во времени.
Определение областей оптимальных значений этих параметров и эксплуатационных характеристик качества изделия является основной проблемой при физико-химических исследованиях и анализе ТП пропитки и заливки в производстве РЭА
5. Электрофизические характеристики соприкасающихся поверхностей и границ раздела слоев
Многолетний опыт производства РЭА на базе кремниевых ИМС показал, что для решения проблем стабильности качества изделий требуется изучение свойств поверхности используемых материалов, а также методов ее подготовки и защиты. Задача становится особенно актуальной в связи с тем, что наиболее перспективными типами РЭА признаны те, которые базируются на полевых приборах (МДП БИС и приборы с барьером Шоттки). Создание же качественных и стабильных приборов этого типа невозможно без знания, свойств поверхностей раздела слоев, образующих их структуры, и умения контролировать эти свойства.
За счет усовершенствования классических методов исследования поверхности (эллипсометрии, электронной микроскопии, оптоэлектронной микроскопии и др.) и использования их для контроля поверхностных свойств рабочих структур приборов и границ разделов слоев в последнее десятилетие получены новые данные о свойствах поверхностей и границ раздела. При этом влияние поверхностных свойств на параметры приборов для различных материалов различно.
По мере совершенствования конструкций ИМС создаются все более тонкие слои полупроводников, диэлектриков и металлов, что увеличивает влияние характеристик поверхности па свойства прибора; при субмикронных толщинах слоев это влияние становится доминирующим. Целью всякого ТП обработки поверхностей в таких важных элементах РЭА, как ИМС, является получение определенных (заданных) электрофизических свойств этих поверхностей с наименьшими затратами. К сожалению, взаимосвязь между электрофизическими параметрами состояния поверхности и технологическими факторами ее обработки ещё мало изучена. Рассмотрим те электрофизические характеристики поверхности и физико-химические факторы, которые влияют на параметры качества микроэлектронных устройств. Большинство рабочих характеристик таких устройств основано на свойствах соприкасающихся поверхностей и границ раздела слоев в системах металл — полупроводник, полупроводник — диэлектрик, металл — диэлектрик — полупроводник и т. п.
Для изучения влияния свойств поверхностей на электрические характеристики указанных систем исследовались различные сочетания материалов слоев и способов обработки поверхностей. Было показано, что характер обработки поверхностей влияет на процессы генерации и рекомбинации носителей заряда, что выражается в изменении вида вольт-амперных, вольт-фарадных и других характеристик структур ИМС.
Характер взаимосвязи физико-технологических факторов обработки поверхности, электрических свойств границ между слоями является сложным. В последние годы методы исследования поверхности были усовершенствованы, с их помощью можно обнаружить моноатомные пленки и отдельные атомы примесных элементов, т. е. идентифицировать как структуру, так и состав поверхности с очень большой точностью. Тем не менее проблема установления количественных связей между электрофизическими свойствами поверхности (границ раздела) и технологическими факторами ее обработки остается нерешенной. Во время обработки поверхности происходят сложные взаимодействия физического и химического характера на атомном уровне газообразных, жидких и твердых частиц, что изменяет концентрацию поверхностных состояний, определяющих электрические свойства поверхностей раздела между слоями в структурах твердотельных радиоэлектронных устройств (ИМС, ПАВ, ПЗС и др.).
Поэтому вопросы получения в ТП заданного состояния поверхности чрезвычайно важны для всей технологии РЭА. В большинстве случаев в реальном производстве, основанном на использовании многократной обработки поверхности, непрерывно оценивают характер изменения поверхностных свойств изделий или полуфабрикатов в зависимости от изменений методов или режимов обработки. По электрофизическим критериям качества поверхности осуществляют поиск оптимальных способов и режимов обработки, оптимальных конструкций технологических установок. Особенно тщательно обрабатывают поверхности тех деталей, на которых будут формироваться рабочие структуры электронных устройств. Важное значение качество поверхности (ее электрофизические свойства) имеет в таких физико-химических технологических процессах как: осаждение диэлектрических и металлических слоев из паровой, газовой и жидких фаз, процессов окисления, эпитаксии, диффузии и др.