| Скачать .docx |
Реферат: Насыщенные альдегиды и кетоны
Альдегиды и кетоны относятся к карбонильным соединениям (содержат группу >С=О) Они имеют общую формулу:
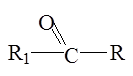 для альдегидов R1
=H.
для альдегидов R1
=H.
Изомерия кетонов связана со строением радикалов и с положением карбонильной группы в углеродной цепи. Кетоны называют по номенклатуре IUPAC называют аналогично альдегидам, но прибавляют окончание -он.
способы получения альдегидов и кетонов
1. Окисление спиртов
R-CH2 -OH + H2 CrO4 ® R-CHO + H2 CrO3 (неустойчива)+ H2 0
2. Дегидрирование спиртов.
(катализатор Cu ):
CH3 OH ® HCOH + H2 O
3. . Гидроформилирование алкенов
CH2 =CH2 + CO +H2 ® CH3 CH2 CHO
Реакция открыта Реленом в 1938г. (100-200о С, 100-250 ат, СО, катализатор – ThO2 +mgoна кизельгуре). Процесс (оксосинтез) катализируется карбонилами кобальта.
Восстановление карбоновых кислот и их производных.

(реакция Роземунда, катализатор – Pd на BaSO4 ).
Если взять смесь солей двух кислот или смешанную соль, то также протекает реакция между молекулами разных солей. Если же одна из солей - формиат, то получается альдегид:

CH3 COOH + HCOOH®CH3 COH
(катализаторы – ThO2 , MnO, CaO, ZnO, 400-450о С).
5. Синтез альдегидов и кетонов через реактивы Гриньяра

Кетоны получают взаимодействием реактивов Гриньяра с нитрилами:
R-CºN + RMgX® (R)2 C=N- Mg+ X + H2 O® (R)2 C=O
химические свойства альдегидов и кетонов
Повышенная реакционная способность связи С=О вызвана различием электроотрицательностей углерода и кислорода. Реакции альдегидов и кетонов могут катализироваться основаниями, кислотами, или и кислотами, и основаниями. Альдегиды и кетоны вступают в реакции присоединения (вода, спирты, HCN, гидросульфит), присоединения - отщепления (аммиак, амины, гидроксиламин, гидразин и его производные) и реакции по a-углеродному атому.
1. Присоединение воды и спиртов
Вода присоединяется к альдегидам и кетонам, образуя неустойчивые гем-диолы:
>C=O + H2 O® >C(OH)2
Устойчивый продукт присоединение воды образуется с хлоралем:
Cl3 CCHO + H2 O®Cl3 CCH(OH)2
хлоральгидрат
Устойчивость образующегося соединения связана с наличием трихлорметильной группы.
Формальдегид также реагирует с водой, образуя гидрат, но в виде гидрата находится лишь 40% альдегида. Такой раствор формальдегида в воде называется формалином.
Спирты, как и вода, реагируют с альдегидами и кетонами:
RCHO + R’OH « RCH(OR’)OH + R’OH « RCH(OR’)2
Возможно образование соединений, содержащих один алкоксильный остаток -OR’ (полуацетали, полукетали) или два - ацетали, кетали. Образование полуацеталей катализируется и кислотами, и основаниями:
Кислотный катализ

Основной катализ
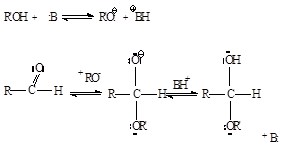
Реакция образования ацеталей (кеталей) катализируется только кислотами. В качестве исходного может быть использован альдегид или полуацеталь. Реакции присоединения спиртов с образованием ацеталей и кеталей являются обратимыми. Они относятся к кислотно-катализируемым реакциям. Ацетали устойчивы к действию оснований.
Активация карбонильной группы в реакциях присоединения воды и спиртов возможна двумя путями: через образование ассоциативных комплексов типа >C=O...HB (водородная связь) или перенос протона, составляющий первую стадию кислотного катализа. Активация посредством образования ассоциативного комплекса называется специфическим катализом, второй путь - общим катализом. В первом случае скорость реакции зависит от рН среды:
Специфический катализ: >C=O + H3 O+ « >C+ ¼OH + H2 O
Общий катализ: >C=O + H-A« >C=O...H...A
2. Присоединение синильной кислоты
Синильная кислота присоединяется к карбонильным соединениям с образованием гем-цианоксидов (циангидринов). Реакция катализируется только основаниями, которые позволяют получить активный нуклеофил CN- из слабой кислоты HCN. Циангидрины встречаются в природе, например, содержатся в косточках сливы, вишни, персика и в миндале. Циангидрины приводят к тяжелому отравлению в результате освобождения синильной кислоты внутри организма.

3. Присоединение бисульфита натрия
Альдегиды и кетоны взаимодействуют с бисульфитом натрия, образуя соли, хорошо растворимые в воде:
RCHO + NaHSO3 ® RCH(OH)SO3 - Na+
Этот метод используют для очистки альдегидов и кетонов. Для выделения их из соли используют разбавленные кислоты и основания.
4. Реакции присоединения - отщепления
Большинство реакций присоединения – отщепления сводится к конденсации карбонильной группы с реагентом типа H2 Z, где Z - остаток молекулы. В результате реакции образуется вода и органическое соединение с группой C=Z вместо С=О. Сначала происходит присоединение по карбонильной связи, а затем – 1,2-отщепление:
>C=O + H2 Z ® >C(OH)ZH ® >C=Z + H2 O
Наиболее обширным классом соединений, которые вступают в реакции присоединения - отщепления, являются аммиак и его производные. Продукты этих реакций содержат связь C=N:

Продукт этой реакции называется иминов или основанием Шиффа. Имины типа >C=NН называются незамещенными иминами, типа >C=NR – замещенными иминами.
Многие другие производные аммиака также дают с альдегидами и кетонами аналогичные продукты конденсации. К таким производным относятся гидроксиламин (NH2 OH), гидразин (NH2 -NH2 ), фенилгидразин (NH2 -NHC6 H5 ) и семикарбазид (NH2 -NHC(O)NH2 ). Продукты их конденсации с карбонильными соединениями называются соответственно оксимами, гидразонами, фенилгидразонами и семикарбазонами:

Конденсацию карбонильных соединений с этими реагентами проводят в присутствии электрофильного катализатора, чаще всего – протона.
Альдольная конденсация.
Под действием каталитических количеств водной кислоты или основания альдегиды превращаются в b-оксиальдегиды. Этот процесс носит название альдольной конденсации:
2 CH3 CHO®CH3 CH(OH)CH2 CHO
ацетальдегид альдоль
Альдольная конденсация, катализируемая основаниями.
Катализируемая основаниями альдольная конденсация начинается с образования енолят-иона альдегида. Поскольку енолят-ион является нуклеофилом, следующей стадией является атака енолят-ионом карбонильной группы другой молекулы альдегида. В результате образуется алкоксид-ион. Далее происходит протонирование алкоксид-иона водой, при этом образуется конечный продукт - альдоль (3) и регенерируется катализатор (ОН - ). Это происходит потому, что алкоксид-ион является более сильным основанием, чем гидроксид-ион.

При нагревании в присутствии основания альдоли легко отщепляют воду, образуя a,b-ненасыщенные альдегиды. Дегидратация протекает легко благодаря кислому характеру атома водорода у a-углеродного атома углерода и вследствие того, что продукт содержит сопряженную систему двойных связей:
CH3 CH(OH)CHCHO®CH3 CH=CHCHO
3-оксибутаналь (альдоль) 2-бутеналь (кротоновый альдегид)
Этот тип конденсации получил название кротоновой .
Альдольная конденсация, катализируемая кислотами
Механизм альдольной конденсации, катализируемой кислотами, включает две основных стадии: превращение кето-формы альдегида в енольную форму и атака образовавшимся енолом карбонильной группы альдегида:

Альдоль под действием разбавленной кислоты отщепляет воду даже при комнатной температуре, поэтому конденсацию, катализируемую кислотой, практически невозможно остановить на стадии b-оксиальдегида:

Кетоны вступают в альдольную конденсацию значительно труднее, чем альдегиды. Однако, при катализе кислотами образующийся в небольших количествах 4-окси-4-метил-пентан-2-он (продукт альдольной конденсации) будет быстро дегидратироваться в 4-метил-3-пентен-2-он (мезитилоксид):
