| Скачать .docx |
Реферат: Газовая хроматография
РЕФЕРАТ
ГАЗОВАЯ ХРОМАТОГРАФИЯ
Москва, 2009
ВВЕДЕНИЕ
Газовая хроматография — наиболее теоретически разработанный метод анализа. Именно развитие теории и практики газовой хроматографии способствовало быстрому развитию в последние десятилетия жидкостной колоночной хроматографии и высокоскоростной жидкостной хроматографии. Отличие метода газовой хроматографии от других хроматографических методов связано с тем, что в качестве подвижной фазы в ней используют газ. В зависимости от агрегатного состояния неподвижной фазы различают газо-адсорбционную хроматографию и газо-жидкостную. Газохроматографическое разделение в таких системах достигается за счет многократно повторяющегося процесса распределения компонентов смеси между движущейся газовой фазой и неподвижной твердой или жидкой фазой, нанесенной на инертный носитель. Процесс разделения основан на различии в растворимости и летучести анализируемых компонентов. Быстрее через хроматографическую колонку движется тот компонент, растворимость которого в неподвижной фазе меньше, а летучесть при данной температуре больше.
Выбор условий получения эффективной колонки в газовой хроматографии вытекает непосредственно из общей теории хроматографического разделения, а выбор селективной стационарной фазы связан с теорией адсорбции и растворения. Различия в коэффициентах распределения компонентов между подвижной и стационарной фазами обусловлены различиями межмолекулярных взаимодействий. Наиболее важными из них являются Ван-дер-ваальсовые взаимодействия. Большую роль также играет такой вид взаимодействий, как водородная связь, причем вклад ее в удерживание значительно уменьшается с ростом температуры. Это может выразиться в изменении порядка выхода разделяемых веществ из колонки при повышении температуры. Комплексообразование для селективного разделения веществ в газовой хроматографии используется реже, чем в жидкостной.
Газовая хроматография бывает элюентная, фронтальная и вытеснительная.
Применение газа в качестве подвижной фазы обусловливает такие преимущества метода, как быстрота проведения анализа, четкость разделения. Анализируемая проба проходит через колонку в виде газа или паров. Этим методом могут быть проанализированы не только газообразные, но и жидкие и твердые вещества. Их анализ возможен при нагревании, что необходимо для переведения веществ в газообразное состояние. Поэтому температура как рабочий параметр процесса играет в газовой хроматографии большую роль, чем в других хроматографических процессах. Рабочие температурные пределы для газо-адсорбционной хроматографии от 70 до 600° С, для газо-жидкостной — от 20 до 400°С. Описана аппаратура для проведения газохроматографических анализов в области температур выше 800°С. В большинстве случаев газохроматографический анализ проводят в изотермических условиях. При анализе веществ с большим разбросом значений температур кипения периодически или непрерывно в процессе анализа повышают температуру. Промышленностью выпускаются приборы для работы с программированием температуры.
Методом газовой хроматографии могут быть проанализированы вещества с молекулярной массой меньше 400. Испарение этих веществ можно провести 'воспроизводимо, т. е. они могут быть переведены в паровую фазу и вновь сконденсированы без изменения состава.
В аналитической практике в основном применяют метод газожидкостной хроматографии. Его преимущества перед газо-адсорбционным связаны главным образом с возможностью широкого выбора неподвижных жидких фаз различной химической природы, а также с высокой чистотой и однородностью жидкостей. Термостойкость адсорбентов дает возможность также проводить разделения высококипящих соединений.
Недостатком газо-адсорбционного метода является нелинейность изотерм адсорбции, приводящая к несимметричности пиков.
ГАЗОХРОМАТОГРАФИЧЕСКИЙ АНАЛИЗ НЕОРГАНИЧЕСКИХ ВЕЩЕСТВ
Развитие методов газовой хроматографии в анализе неорганических веществ отстает по сравнению с газовой хроматографией органических веществ. Во-первых, это связано с агрессивностью многих неорганических соединений по отношению к адсорбентам, неподвижным фазам и к материалам, из которых изготовляется обычно аппаратура для проведения газохроматографических анализов. Во-вторых, газовая хроматография неорганических веществ начала развиваться позже, чем газовая хроматография органических соединений. Это обусловлено тем, что для анализа неорганических веществ имеются классические методы, превосходящие по точности и скорости методы анализа органических соединений. Однаио уже в настоящее время газовая хроматография позволяет анализировать соединения почти всех элементов периодической системы.
ТРЕБОВАНИЯ К АНАЛИЗИРУЕМЫМ ВЕЩЕСТВАМ
Газохроматографическим методом могут быть проанализированы не любые вещества, а только удовлетворяющие определенным требованиям, главные из которых перечислены ниже.
1. Летучесть. Достаточно, чтобы упругость пара вещества при рабочей температуре колонки была невысокой. Более летучим считается вещество, упругость паров которого выше, чем у другого. Наличие больших моментов диполя, поляризация, водородная связь приводят к уменьшению летучести; ионные и сильнополярные соединения нелетучи.
2. Стабильность. Количественный анализ вещества возможен, если оно испаряется в дозаторе и элюируется без разложения, т. е. является термостойким. При разложении веществ на хроматограмме появляются ложные пики, присущие продуктам разложения, что приводит к ошибкам в анализе. Возможен анализ соединений, для которых отработана методика воспроизводимого разложения.
3. Инертность. Вещество не должно образовывать прочных сольватов при растворении в жидкой стационарной фазе, не должно реагировать с материалами, из которых изготовлены детали хроматографа.
4. Легкость получения. При проведении количественного анализа желательно работать с такими соединениями, которые легко получить с количественным выходом.
Этим требованиям в большей мере, как правило, удовлетворяют органические вещества. Однако в последние годы разработаны способы газохроматографического анализа различных металлов и их неорганических и органических соединений.
АНАЛИЗ МЕТАЛЛОВ И ИХ СОЕДИНЕНИЙ
Анализ свободных металлов возможен при использовании сверхвысокотемпературной хроматографической аппаратуры. Соединений металлов, летучих при сравнительно низких температурах, немного: галогениды, алкоголяты, различные хелаты, гидриды.
Свободные металлы. Разработаны методы хроматографирования свободных металлов при сверхвысоких тысячеградусных температурах. Например, удалось осуществить прямое газохроматографическое определение цинка, кадмия и магния в сплавах типа припоев и легких сплавах на основе олова, свинца и висмута без химической обработки. Разделены цинк, кадмий и ртуть в виде паров этих металлов. Металлические калий и натрий разделить в виде паров пока не удалось; они элюируются вместе при 600—10000 C. В будущем прямое газохроматографическое разделение металлов может быть использовано при очистке металлов и их сплавов от ультрамалых количеств примесей.
Гидриды металлов. В ряде работ осуществлен газохроматографический анализ летучих гидридов металлов. Возможно непосредственное разделение гидридов сурьмы, олова, титана, ниобия и тантала. При хроматографировании гидридов металлов следует учитывать их высокую реакционную способность, склонность к гидролизу и легкую окисляемость. Газохроматографический анализ гидридов возможен лишь при отсутствии кислорода в системе.
Галогениды металлов. Газохроматографическим методом могут быть разделены и количественно определены галогениды переходных металлов. Разделение летучих хлоридов можно осуществить методом термохроматографии в сочетании с комплексообразованием. Описано разделение летучих хлоридов Sb, Sn, In, Cd, Zr, Hf, Nb, Ta, Mo, Tc, Re, Ru, Os методом термохроматографии с использованием температурного градиента от 600 до 25°С. При значительно более низких температурах возможно определение хлоридов галлия, германия, мышьяка, сурьмы и кремния. Основная трудность, возникающая при хроматографии галогенидов металлов,— их высокая реакционная способность. В колонке при повышенной температуре они реагируют со многими жидкими неподвижными фазами, с металлическими поверхностями деталей хроматографа, в том числе колонок. Галогениды легко гидролизуются, поэтому из газа-носителя следует удалять даже следы влаги. Поскольку адсорбенты часто более инертны, чем жидкие неподвижные фазы, то при анализе галогенидов металлов метод газо-адсорбционной хроматографии имеет определенные преимущества по сравнению с методом газо-жидкостной хроматографии.
Из всевозможных соединений металлов, используемых для газохроматографического анализа, наибольший практический интерес представляют хелаты. Можно получить хелаты практически любого металла. В настоящее время синтезировано много хелатов, летучесть и термическая стойкость которых удовлетворяют требованиям газовой хроматографии. Получить хелаты металлов с количественным выходом можно либо при взаимодействии хлоридов металлов с соответствующими лигандами, либо при непосредственной обработке металла или его оксида хелатообразующим реагентом. Это знательно упрощает и ускоряет анализ. Поэтому чрезвычайно удобно использовать хелаты металлов с получают новые лиганды, способные давать прочные летучие хелаты с металлами:
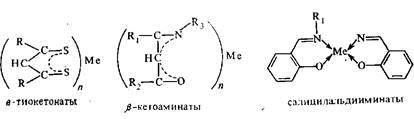
Следует отметить, что предел обнаружения хорошо хроматографирующихся хелатов составляет несколько пикограммов и зависит от чувствительности детектора. Для плохо хроматографирующихся хелатов предел обнаружения составляет несколько микрограммов.
Связь летучести хелатов со структурой их молекул. Для целенаправленного синтеза летучих хелатов металлов были предприняты попытки теоретически обобщить накопленный экспериментальный материал по их хроматографическому поведению.
Попытки связать конфигурацию молекулы комплекса с летучестью или хроматографичностью пока не дали однозначных результатов. Известны летучие и хорошо хроматографирующиеся комплексы, имеющие тетраэдрическую, октаэдрическуюи плоскоквадратнуюконфигурации. В то же время многие комплексы такой же конфигурации мало летучи или плохо хроматографируются.
Известны как стабильные, так и лабильные летучие комплексы, т. е. не вполне ясен вопрос о роли кинетической стабильности комплексов.
Большинство известных летучих комплексов содержит либо шестичленные циклы с делокализованной двойной связью, либо четырехчленные циклы с делокализованной двойной связью. Практически неизвестны летучие хелаты с пятичленным циклом.
К настоящему времени установлено, что структура комплекса влияет на его хроматографическое удерживание. Удерживание изоструктурныхв-дикетонатов разных металлов с одним и тем же лигандом возрастает с увеличением радиуса иона металла. Однако удерживание аналогичных по структуре хелатов различных металлов в большей мере обусловлено лигандом и используемой жидкой фазой. При небольших различиях ионных радиусов металлов можно подбором жидкой фазы изменить порядок выхода хелатов из колонки. Так, при хроматографировании в-кетоаминатов никеля и меди на колонке с полиметилтрифторпропил-силоксаном QF-I хелат никеля выходит из колонки раньше хелата меди. На колонке с апиезоном L эти хелаты выходят одновременно, а на колонке с поликарборансилоксаном в.-кетоаминат меди выходит раньше соответствующего хелата никеля. Часто многие экспериментально наблюдаемые факты можно объяснить только специфическим взаимодействием молекул хелатов металлов с жидкой фазой, однако природа этого взаимодействия во многих случаях недостаточно ясна.
Механизм удерживания хелатов. В ряде работ исследовался механизм удерживания хелатов металлов. Было установлено, что удерживание ряда хелатов определяется тремя главными факторами: 1) растворением в жидкой фазе; 2) адсорбцией на поверхности твердой фазы; 3) адсорбцией хелата на поверхности жидкой фазы.
Газовая хроматография с модифицированной подвижной фазой. Для разделения комплексов металлов разработаны два метода, использующие газовую хроматографию с модифицированной подвижной фазой.
В одном из них используется носитель, содержащий лары лиганда. Разложение и сорбцию в-дикетонатов металлов в колонках уменьшают добавлением в таз-носитель небольшого количества паров соответствующего в-дикетона. Термодинамические характеристики системы при этом не меняются. Улучшение хроматограмм объясняется подавлением диссоциации хелатов в жидкой фазе в присутствии избытка свободного в-дикетона. В таких условиях удалось полностью разделить ряд хелатов соседних в таблице Д.И. Менделеева РЗЭ. Этот метод пока не удалось распространить на другие летучие комплексы металлов, такие, как ди-этилдитиокарбаминаты, диалкилдитиофосфаты и диалкилдитио-фосфинаты.
Во втором методе предлагается использовать три высоких давлениях в качестве подвижной фазы фреон в сверхкритическом состоянии. При этом летучесть многих комплексов металлов увеличивается за счет изменения термодинамических параметров системы. Метод не нашел широкого практического применения из-за сравнительной сложности аппаратуры.
Следует отметить, что большие трудности в газовой хроматографии хелатов металлов связаны с аномалией в поведении многих из них в хроматографической колонке, причем аномальное поведение резко усиливается при переходе к очень малым количествам.
ОПРЕДЕЛЕНИЕ ВОДЫ
Содержание воды в веществах различного агрегатного состояния можно определять методами газо-жидкостной, газо-адсорбционной и реакционной газовой хроматографии. Самым быстрым и часто наиболее удобным способом определения воды в неорганических и органических материалах является метод газо-адсорбционной хроматографии на колонках с пористыми полимерными сорбентами или углеродными молекулярными ситами. Метод газо-жидкостной хроматографии для определения воды менее пригоден. При использовании «акполярных, так и неполярных жидких фаз, нанесенных на диатомитовые носители, пики воды получаются несимметричными, в первом случае — из-за сильного взаимодействия воды с гидроксильными группами поверхности носителя, а во втором — из-за образования прочных водородных связей между молекулами полярной неподвижной фазы и молекулами воды. Наиболее симметричные пики воды были получены на насадке, состоящей из тефлона и различных полиэтиленгликолей, т.е. при использовании совершенно инертного носителя неподвижной жидкой фазы.
Часто содержание воды определяют косвенными методами, применяя реакционную газовую хроматографию. Вода реагирует с гидридами металлов, карбидом кальция, металлическим натрием и т. д., продукты реакции детектируются пламенно-ионизационным детектором.
ДОСТОИНСТВА И ОБЛАСТИ ПРИМЕНЕНИЯ ГАЗОВОЙ ХРОМАТОГРАФИИ
Метод газовой хроматографии является одним из самых современных методов анализа. Его отличительные черты — экспрессность, высокая точность, чувствительность, возможность автоматизации. С помощью этого метода могут быть решены многие аналитические проблемы выбором хроматографической системы и рабочих условий. Широкий набор стационарных жидких фаз и адсорбентов, с одной стороны, программирование температуры, высокое давление, специфические методы детектирования, с другой стороны, позволяют разделять и количественно определять соединения с едва заметной разницей в давлении пара. Степень универсальности и гибкости метода газовой хроматографии во многом определяется существующим техническим уровнем аппаратуры. Если в качественной газовой хроматографии надежная идентификация компонентов смеси может быть чаще всего обеспечена лишь сочетанием с другими независимыми аналитическими методами, то количественный газохроматографический анализ может рассматриваться как самостоятельный аналитический метод, дающий результаты, не вызывающие сомнений.
Газовая хроматография используется также в препаративных целях для очистки химических препаратов, выделения индивидуальных веществ из смесей. Метод особенно эффективен при разделении веществ, относящихся к одному и тому же классу — углеводородам, органическим кислотам, спиртам и т. д.
Метод широко применяется в физико-химических исследованиях: для определения физико-химических свойств адсорбентов, для определения термодинамических характеристик адсорбции, теплоты адсорбции, 'поверхности твердого тела и термодинамических свойств растворов — констант равновесия, изотерм распределения, коэффициентов активности и др.
Следует отметить, что метод непрерывно развивается и совершенствуется. Расширяются и границы применимости метода в различных областях науки и техники. В химии и нефтехимии это анализ нефти и продуктов ее переработки: анализ смесей газообразных углеводородов; анализ бензина, воска и продуктов их окисления; изучение серо- и азотсодержащих продуктов крекинга; анализ растворителей — спиртов, кетонов, смесей углеводородов; изучение состава природных продуктов. В сельском хозяйстве это анализ гербицидов, пестицидов, удобрений.
Развитие метода идет по пути синтеза новых хелатов металлов, достаточно летучих и устойчивых в условиях хроматографирования, а также в направлении поиска вое более чувствительных и селективных детектирующих систем для комплексных соединений металлов с органическими лигандами.
Метод газовой хроматографии незаменим в металлургии, энергетике, биологии, медицине, в пищевой промышленности, используется для управления технологическими процессами.