| Скачать .docx | Скачать .pdf |
Реферат: Адсорбция полимеров
Содержание
1. Взаимодействие полимеров с твердыми поверхностями
1.1 Адсорбция и молекулярная масса полимера
2. Влияние растворителя на адсорбцию
3. Электростатические взаимодействия и адсорбция
1. Взаимодействие полимеров с твердыми поверхностями
Адсорбция полимеров широко используется во многих технологических системах: в дисперсиях частиц, в процессах флокуляции, при обработке твердых поверхностей и т.д. В этих процессах адсорбцию полимера проводят для модифицирования взаимодействий между поверхностями. С термодинамической точки зрения главной движущей силой адсорбции полимера является сильное взаимодействие полимерных сегментов с поверхностью, например при адсорбции катионных полимеров на анионной поверхности. В плохом растворителе наблюдается сильное эффективное притяжение между полимером и твердой поверхностью. Полимер стремится использовать все возможности для устранения контакта с растворителем и, следовательно, адсорбируется практически на любой поверхности, даже на поверхности жидкость-воздух. Адсорбция полимера на поверхности в этом случае всегда предшествует его осаждению из раствора. Поверхности, присутствующие в системе, действуют как активные центры для осаждения полимера. Основной вывод сводится к тому, что чем хуже взаимодействие растворитель-полимер, тем выше адсорбция, и наоборот.
Полимеры с большой молекулярной массой обладают более выраженной склонностью к адсорбции, чем полимеры с меньшими молекулярными массами. Отсюда вытекает много следствий. Во-первых, типичный вид изотермы адсорбции полимеров: характерно резкое увеличение адсорбции при очень низких концентрациях с последующим плато, когда адсорбция не меняется с концентрацией полимера. Очень сильная адсорбция при низких концентрациях отражает "дискомфорт" полимера в растворе из-за слабого взаимодействия полимер-растворитель. Этот эффект еще сильнее проявляется при возрастании молекулярной массы полимера. Постоянство адсорбции при более высоких концентрациях свидетельствует о насыщении поверхности полимером.
При измерении изотерм адсорбции полимеров из раствора важно помнить, что для достижения равновесия требуется определенное время. Обычно при осторожном перемешивании для достижения адсорбционного равновесия требуется около 24 часов.
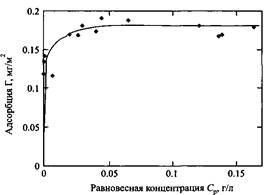
Рис.1. Изотерма адсорбции полиакриловой кислоты из водного раствора на каолине иллюстрирует основные особенности адсорбции полимеров: резкое увеличение адсорбции при низких концентрациях полимера и постоянную адсорбцию при больших концентрациях
Но иногда необходимо и более длительное время, особенно для пористых твердых тел, поскольку при этом полимер диффундирует в поры, где еще остаются свободные центры адсорбции.
Известно, что иногда полиэлектролитом называют любой агрегат с большим зарядом. В то же время в специальной литературе этот термин относят к заряженным полимерам, и именно этот тип полиэлектролитов рассмотрен ниже. Результирующий заряд гибкого полимера формируется за счет карбоксилат - или сульфат-ионов, аминогрупп или аналогичных азотсодержащих соединений. Полиэлектролиты делят на сильные и слабые; заряд последних зависит от рН. Зависимость заряда полиэлектролитов от рН может быть очень сложной, что отражается на изотермах адсорбции. Электростатические взаимодействия влияют на процесс адсорбции, несмотря на превалирующую роль взаимодействий не электростатической природы.
1.1 Адсорбция и молекулярная масса полимера
Анализ зависимостей количества адсорбированного полимера от молекулярной массы привел к пониманию того, как полимер адсорбируется на поверхности твердого тела. В том случае, если полимер лежит плоско на поверхности, адсорбция не должна зависеть от молекулярной массы. Если же полимер при адсорбции закрепляется на поверхности только концом цепи, адсорбция прямо пропорциональна молекулярной массе. На самом деле для большинства полимеров установлено, что полимеры адсорбируются в конформации клубка, и количество адсорбированного полимера пропорционально величине Ma , где M - молекулярная масса, а б - константа, значение которой обычно лежит в пределах 0.3-0.5. Типичная картина, отражающая зависимость адсорбции полимера от молекулярной массы на примере адсорбции поливинилового спирта из водных растворов на поверхности полистирольного латекса, показана на рис.2. Существенно, что при низких концентрациях адсорбция растет все резче при увеличении молекулярной массы полимера. В противоположность этим результатам адсорбция полиоксиэтилена из водных растворов на кремнеземе происходит совершенно иначе. В этой системе адсорбция не зависит от молекулярной массы. Причина этого, по-видимому, заключается в высоком сродстве эфирных групп полимера к гидроксильным группам, расположенным на поверхности кремнезема, что приводит к плоской конфигурации полимера на поверхности.
Чем больше молекулярная масса полимера, тем сильнее он адсорбируется. Таким образом, при адсорбции полидисперсного образца полимера в первую очередь адсорбируются высокомолекулярные фракции, оттесняя низкомолекулярные фракции с поверхности. Для примера на рис.3, а приведены изотермы адсорбции) смесей двух полимеров с различными молекулярными массами. Здесь же приведены изотермы адсорбции индивидуальных полимеров. Изотерма адсорбции из бинарного раствора полимеров имеет три участка. На первом участке при очень низкой концентрации полимеров поверхности адсорбента достаточно, чтобы количественно адсорбировать весь полимер. Далее при повышении концентрации полимеров бинарная смесь полимеров покрывает всю поверхность, и начинается обменный процесс, при котором более высокомолекулярный компонент вытесняет с поверхности низкомолекулярный. И, наконец, при более высоких концентрациях полимера в смеси высокомолекулярный компонент покрывает всю поверхность адсорбента, и достигается практически постоянная его адсорбция.
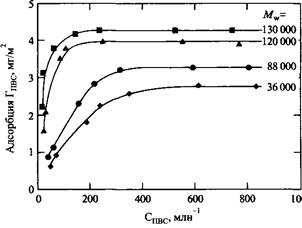
Рис.2. Адсорбция поливинилового спирта на поверхности полистирола при различных молекулярных массах ПВС

Рис. 3. а - Адсорбция двух декстранов с молекулярными массами 9000 и 500000 г/моль соответственно и их смеси при соотношении 50: 50. Все полимеры адсорбируются при низких концентрациях, в случае смесей на изотерме наблюдается участок, на котором происходит вытеснение с поверхности полимера с низкой молекулярной массой полимером с высокой молекулярной массой. б-Влияние соотношения поверхность: объем на адсорбцию полимеров из смеси 50: 50. Сплошные и пунктирные кривые относятся к малым и большим отношениям поверхность: объем соответственно
Поскольку количество адсорбированного полимера зависит от молекулярной массы, измеряемая величина адсорбции зависит от соотношения объема раствора полимера и доступной площади поверхности адсорбента. Небольшая доступная площадь поверхности адсорбирует только высокомолекулярные компоненты, и при этом регистрируется большая адсорбция. При большой площади поверхности адсорбируются и компоненты с более низкими молекулярными массами, а регистрируемая величина адсорбции полимера при этом оказывается более низкой. Проблему можно преодолеть изменением переменной Cp с учетом следующего соотношения:
![]()
где V - объем раствора, А - общая доступная площадь поверхности. Из рис.3, б видно, что адсорбция на втором участке, когда высокомолекулярные компоненты вытесняют низкомолекулярные, зависит от соотношения поверхности и объема. Этот участок изотермы адсорбции распространяется в область более высоких концентраций полимера при высоком соотношении Al V, т.е. когда в системе имеется достаточно большая поверхность. При замене концентрации полимера на Гь получается одна кривая.
2. Влияние растворителя на адсорбцию
Взаимодействие растворитель-полимер, или качество растворителя, влияет на адсорбцию полимера двумя путями. Во-первых, взаимодействие растворитель-полимер определяет конформацию полимера в растворе. Как обсуждалось ранее, полимерная молекула принимает развернутую конформацию в хороших растворителях и сжимается в плохих. Поэтому полимер, адсорбирующийся из хорошего растворителя, занимает на поверхности большую площадь, а из плохого растворителя - меньшую площадь. В связи с этим адсорбция полимера из плохих растворителей всегда выше. Во-вторых, растворитель влияет на адсорбцию через устойчивость раствора, и, как уже говорилось, при "дискомфортности" полимера в растворе он использует любую возможность для устранения контакта с растворителем, включая адсорбцию на поверхности. В таблице 1 приведены данные по адсорбции на угле полистирола из метилэтилкетона, в который добавляли метанол. Из таблицы следует, что количество адсорбированного полимера увеличивается по мере приближения к точке осаждения полимера из раствора. Этот факт также подтверждает, что поверхность выполняет роль зародыша осаждения и что адсорбция усиливается перед осаждением.
Таблица 1. Адсорбция полистирола на угле
| Концентрация метанола в метилэтилкетоне,% | Адсорбция, мг/г |
| 0 | 34 |
| 0.5 | 35 |
| 1.0 | 48 |
| 1.5 | 46 |
| 2.5 | 81 |
| 5.0 | 144 |
| 10.0 | 144 |
| 12.3 | осаждение |
Адсорбция водорастворимых полимеров на твердых поверхностях действительно определяется свойствами раствора полимера. Это положение иллюстрирует рис.4 на примере адсорбции этилцеллюлозы на кремнеземе. На рис.4, а приведена зависимость точки помутнения раствора от концентрации различных добавленных солей, а на рис.4, б-зависимость адсорбции на кремнеземе в присутствии тех же солей. Из сравнения этих рисунков явствует, что соли, понижающие точку помутнения, т.е. понижающие растворимость ЭГЭЦ, повышают ее адсорбцию. Таким образом, адсорбция является мерой стремления полимера уйти из раствора. Аналогичным образом соли, повышающие точку помутнения и увеличивающие растворимость полимера, понижают его адсорбцию. Подчеркнем, что этот эффект не связан именно с добавками солей, а является общей закономерностью адсорбции полимеров.
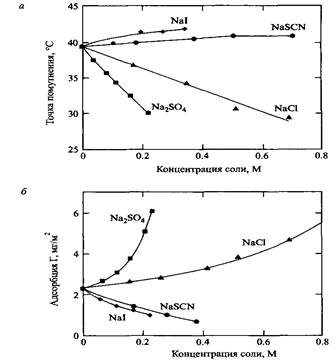
Рис. 4. а - Зависимость точки помутнения водных растворов эталцеллюлозы от концентрации соли; б - адсорбция ЭГЭЦ из тех же растворов на поверхности кремнезема. Данные показывают, что адсорбция увеличивается по мере уменьшения растворимости ЭГЭЦ
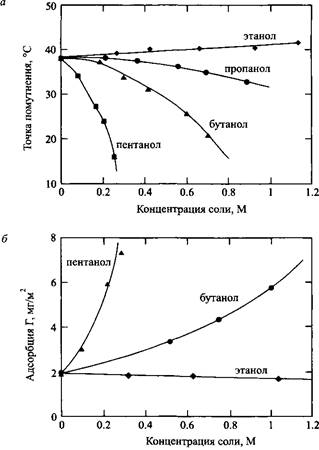
Рис.5. а - Зависимость точек помутнения от концентрации соли в системе водный раствор ЭГЭЦ-спирт; б - адсорбция ЭГЭЦ из тех же растворов на поверхности кремнезема. Результаты показывают, что адсорбция ЭГЭЦ повышается при уменьшении ее растворимости
На рис.5, б и б показаны результаты измерений адсорбции ЭГЭЦ на кремнеземе в присутствии различных спиртов. Видно, что добавки, уменьшающие растворимость и понижающие точку помутнения, также приводят к увеличению адсорбции, и наоборот.
3. Электростатические взаимодействия и адсорбция
Адсорбцию полиэлектролитов на поверхности твердых тел можно разделить на три типа. Здесь показаны зависимости заряда поверхности и полиэлектролита от рН. Общая закономерность такова, что заряд положителен при низких значениях рН и отрицателен при высоких значениях рН. Конечно, кривые могут также стремиться к нулевому заряду либо в кислой области рН, либо в щелочной. На рисунке показаны различные области, когда полиэлектролит и поверхность несут противоположные заряды или заряжены одноименно.
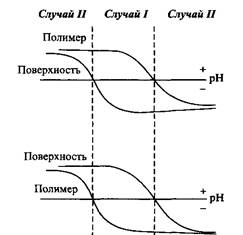
Рис.6. Схематическое представление изменения заряда полиэлектролита и поверхности в зависимости от рН для двух случаев, когда рК полимера больше и меньше рК поверхности
В первом случае разноименно заряженных полиэлектролита и поверхности, на первый взгляд, кажется очевидным, что движущей силой адсорбции является электростатическое притяжение между полиэлектролитом и поверхностью. Поскольку противоионы тоже притягиваются к поверхности и к полиэлектролиту, это положение не столь очевидно. На самом деле движущая сила определяется присутствием противоионов. При адсорбции полиэлектролита на противоположно заряженной поверхности противоионы высвобождаются как с поверхности, так и от полиэлектролита и уходят в раствор. Это приводит к увеличению энтропии системы, в результате чего система переходит в состояние с более низкой свободной энергией. В этом и заключается движущая сила адсорбции полиэлектролита на поверхности, несущей противоположный заряд. На этом основании можно предсказать уменьшение адсорбции полиэлектролита при добавлении соли, поскольку выигрыш в энтропии от высвобождения противоионов в этом случае меньше по сравнению с системами в отсутствие соли. Существует также альтернативная точка зрения, что добавленная соль экранирует полимер и поверхность, уменьшая электростатические силы притяжения между ними. По другим представлениям, введенная в систему соль конкурирует с полиэлектролитом за адсорбционные центры на поверхности твердого тела.
Во втором случае, когда полимер и поверхность заряжены одноименно, движущая сила адсорбции определяется ван-дер-ваальсовыми силами притяжения между полимером и поверхностью.
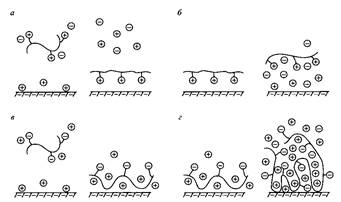
Рис.7. Адсорбция полиэлектролита, соответствующая двум случаям, представленным на Рис.6, и влияние соли на адсорбцию
Интересно отметить, что в этом случае добавление солей приводит к противоположному по сравнению с первым случаем эффекту - увеличению адсорбции. Одна из точек зрения относительно механизма адсорбции заключается в том, что в растворе в отсутствие соли локальная концентрация противоионов увеличивается при адсорбции. Локальное увеличение концентрации противоионов является в определенном смысле "упорядочением" системы, что соответствует уменьшению энтропии и повышению свободной энергии системы. Таким образом, присутствие противоионов препятствует адсорбции полиэлектролита на одноименно заряженной поверхности. Добавление соли снижает этот эффект, приводя к увеличению адсорбции полиэлектролита из-за нивелирования действия противоионов. По альтернативному механизму введение соли вызывает экранирование полимера и поверхности и уменьшение сил отталкивания между ними, а также между различными молекулами полимера, приводя в итоге к повышению адсорбции полимера.
Обсудим некоторые яркие примеры адсорбции полиэлектролитов на заряженных поверхностях. Из таблицы 2 видно, как изменяется адсорбция полиакриловой кислоты на каолине при введении соли. На примере добавок NaCl можно отметить, что адсорбция увеличивается с увеличением ионной силы. Это означает, что адсорбция происходит в системе, отвечающей случаю II. Так как полиакриловая кислота заряжена отрицательно, можно заключить, что адсорбция происходит на одной из отрицательно заряженных плоскостей частичек каолина.
Таблица 2. Адсорбция полиакриловой кислоты из водного раствора на каолине при различных значениях ионной силы
| Электролит | Концентрация | Ионная сила, | Адсорбция, |
| электролита, M | M | мг/м2 | |
| NaCl | 0.20 | 0.20 | 0.18 |
| NaCl | 0.01 | 0.01 | 0.08 |
| CaCl2 | 0.0033 | 0.01 | 0.30 |
Введение соли двухзарядного катиона, например CaCh, приводит к гораздо более сильному увеличению адсорбции полиакриловой кислоты по сравнению с NaCl, поскольку двухзарядный катион обладает более сильной способностью экранировать заряды на полимере и каолине, тем самым уменьшая их отталкивание. Как отмечалось выше, объяснить это явление можно также увеличением энтропии противоионов. При увеличении концентрации соли выигрыш энтропии от растворения полиэлектролита уменьшается, что делает адсорбцию более выгодной. Энтропийный эффект сильнее проявляется в случае двухзарядных ионов, например Ca, просто потому, что уменьшается число кинетических единиц. Другими словами, соли двухзарядных катионов снижают невыгодные локальные концентрации ионов на полиэлектролите при адсорбции. В присутствии трехзарядных и других многозарядных ионов растворимость полиэлектролита уменьшается еще сильнее, и адсорбция увеличивается. Существует и другое мнение, состоящее в том, что введение солей приближает раствор полиэлектролита к фазовому разделению, а следовательно, усиливает адсорбцию.
Начальная стадия адсорбции полиэлектролита является быстрым процессом, однако достижение истинного равновесного состояния происходит очень медленно, что связано с перестройкой и адсорбцией-десорбцией компонентов с различными молекулярными массами. Измерения поверхностных сил показывают, что этот процесс может продолжаться несколько дней и более.
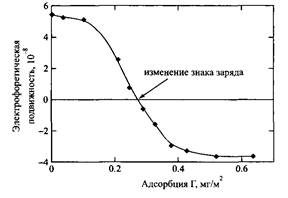
На рис.8 представлена адсорбция катионного полимера на монтмориллоните. Видно, что как только поверхность становится нейтральной, дальнейшая адсорбция прекращается из-за взаимного отталкивания цепей. Максимальная адсорбция отвечает электронейтральной цепи. Этот пример показывает, как электростатические взаимодействия приводят к уменьшению адсорбции, несмотря на то, что полимер и поверхность заряжены разноименно. Очевидно, что адсорбция полиэлектролита зависит также от рН раствора, что определяется зависимостями от рН зарядов поверхности или полиэлектролита. Рисунок 9 иллюстрирует такую ситуацию на примере адсорбции белка: при увеличении рН от изоточки отрицательный заряд белка становится все большим по абсолютной величине. Увеличение плотности заряда поверхности обычно приводит к увеличению адсорбции, поскольку система стремится к электронейтральности. Однако во многих случаях процесс адсорбции контролируется не электростатическими силами, что проявляется при адсорбции отрицательно заряженных цепей на отрицательно заряженных поверхностях. Из рисунка 11 видно, что при введении соли адсорбция увеличивается по мере усиления экранирования и уменьшения отталкивания между цепями при высоких концентрациях соли. Иногда при адсорбции анионного полимера на положительно заряженной поверхности может происходить изменение знака заряда поверхности. Такой пример показан на рис.12 для адсорбции поли на частицах полистирола.

Рис.8. Изотермы адсорбции катионного полимера на отрицательно заряженной поверхности монтмориллонита. Зависимости показывают, как адсорбция изменяется с изменением степени ионизации
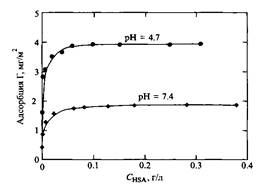
Рис.9. Изотермы адсорбции сывороточного альбумина человека на поверхности отрицательно заряженных частиц золя AgI; концентрация соли 10 мМ; T= 295 К
При планировании эксперимента по определению адсорбции полиэлектролитов из солевого раствора нужно проявлять осторожность. Необходимо контролировать отношение поверхность/объем, так как соль адсорбируется совместно с полимером. При измерении адсорбции в системе с небольшой доступной площадью поверхности адсорбирующаяся совместно с полимером соль присутствует в избытке. При проведении эксперимента в системе с большой доступной площадью поверхности появляется риск того, что вся соль, присутствующая в системе, участвует в совместной адсорбции с полимером. Тогда фактором, определяющим адсорбцию полимера, становится не его растворимость, а доступность в данной системе соли. Это положение иллюстрирует рис.13 на примере адсорбции карбоксиметилцеллюлозы на каолине из водных растворов, содержащих 0.0033 MCaC5 при двух разных количествах адсорбента в системе. При более высоком содержании твердого адсорбента наблюдается уменьшение адсорбции карбоксиметилцеллюлозы из-за присутствия ионов кальция, адсорбция которых приводит к уменьшению их концентрации в растворе.
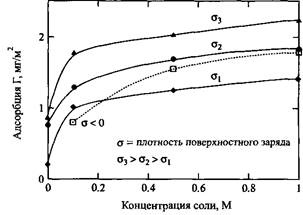
Рис.10. Зависимость адсорбции полистиролсульфоната на положительно заряженных поверхностях с различной плотностью заряда от концентрации соли в растворе
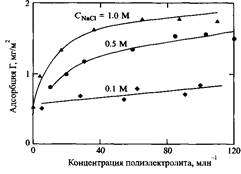
Рис.11. Изотермы адсорбции полистиролсульфоната на отрицательно заряженных поверхностях
Можно придти к заключению, что для получения достоверных результатов при измерении адсорбции полимеров необходимо контролировать следующие параметры: молекулярную массу полимера и распределение по молекулярным массам в образце, рН, ионную силу, наличие многозарядных ионов, а также небольших количеств добавок, отношение площади к объему и температуру.
 |
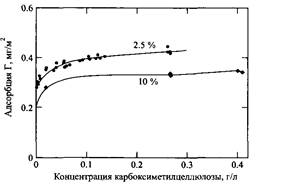 |
Рис.13. Изотермы адсорбции карбоксиметилцеллюлозы на каолине. Адсорбция из водных растворов, содержащих 0.0033 MCaCl2 , при двух разных содержаниях твердого адсорбента
Для оценки конформации макромолекулы на поверхности полезно пользоваться следующими критериальными значениями адсорбции. При поверхностных концентрациях ниже 1 мг/м2 макромолекула располагается на поверхности плоско, при поверхностных концентрациях, близких к 3 мг/м, молекулы полимера в монослое на поверхности адсорбента находятся в конформации клубка. И, наконец, при поверхностных концентрациях выше 5 мг/м2 полимеры адсорбируются либо в виде агрегатов, либо с образованием мультислоев. Конечно, приведенные значения приблизительны, при этом подразумевается, что вся поверхность доступна для адсорбции полимера.