| Скачать .docx | Скачать .pdf |
Реферат: Модели системы кровообращения
Реферат на тему:
"Модели системы кровообращения"
Выполнила
студентка 3-го курса 5-ой группы
факультета математики, механики
и компьютерных наук
Самышкина Ирина.
Модели системы кровообращения
Опыт математического моделирования систем кровообращения насчитывает уже несколько десятилетий, и некоторые из разработанных моделей с успехом применяются в клинической практике. Здесь, очевидно, наибольший интерес представляют модели системы кровообращения в целом, описывающие изменение основных параметров (давление, объем, кровоток) в различных точках системы и допускающие включение в модельные соотношения таких внешних факторов, как измененная весомость и перепад давлений по поверхности тела, обусловленный применением средств компенсации. [1]
Моделирование органов и структур человеческого организма дает возможность предсказать критические ситуации, выяснить механизмы формирования патологии, находить области допустимых изменений формы, механических свойств и характера функционирования этих биологических объектов. Это в свою очередь расширяет сферу применения диагностических методов и устройств и является предпосылкой для создания автоматизированных средств диагностики.
Модель - это объект любой природы, умозрительный или материально реализованный, который воспроизводит явление, процесс или систему с целью их исследования или изучения.
Моделирование - метод исследования явлений, процессов и систем, основанный на построении и изучении их математических или физических моделей
Математическое моделирование биологических объектов представляет собой аналитическое описание идеализированных процессов и систем, адекватных реальным.
Создание физических моделей основано на воспроизведении физическими способами биологических структур, их функций и процессов. При физическом моделировании решают вопросы выбора вида и параметров модели и устанавливают различные виды соответствия между моделью и биологическим объектом.
Модель дает значительно больше информации о биомеханике биологического объекта, чем можно получить современными средствами измерений. [2]
Большое количество различных моделей было разработано для того, чтобы достигнуть лучшего понимания характера соотношений между физическими явлениями, происходящими в артериальном русле человеческого организма, такими, как изменение давления, распространение волн в потоке, и собственными свойствами артерий, такими, как их радиус, толщина стенок, упругость, характер ветвлений, т.е. строением артериального древа как целого.
Весь спектр моделей кровообращения можно разделить на два основных класса. К первому из них относятся модели с распределенными параметрами, в которых рассматривается изменение параметров во времени в каждой точке моделируемого пространственного объекта. Однако, если говорить о моделировании системы кровообращения в целом, решение десятков уравнений в частных производных даже при современном уровне средств программирования и вычислительной техники, представляется крайне трудным и нецелесообразным.
Действительно, с точки зрения некоторых задач наиболее важным представляется аналитическое описание различий параметров между крупными участками системы, например, сосудистой системой мозга и аортой. В то же время тонкими механизмами распространения пульсовой волны явно можно пренебречь, в частности и потому, что для некоторых задач важны процессы с постоянными времени порядка 1с и более.
Второй класс моделей составляют модели с сосредоточенными параметрами, в которых описываемый объект разбивается на несколько участков, и предлагается, что внутри каждого из них все параметры изменяются только во времени, но не в пространстве. Математическая сторона проблемы при таком подходе существенно упрощается и сводится к решению системы алгебраических и обыкновенных дифференциальных уравнений. В то же время при правильном выборе способа разбиения системы на "точечные" участки не будут потеряны локальные особенности, существенные с точки зрения практики. Очевидно, например, что исследование гидростатических эффектов в нижней конечности невозможно, если она не разбита, по крайней мере, на два последовательных элемента, смещенных друг относительно друга вдоль направления вектора перегрузки.
Иначе говоря, модели системы кровообращения обычно делят на две основные группы:
модели гемодинамики сердечно-сосудистой системы;
модели регуляции сердечного выброса.
Модели гемодинамики отражают процессы в отдельных участках (например, в крупных сосудах) системы кровообращения. Они строятся, как правило, на основе прямой аналогии с электрическими цепями, либо косвенной аналогии при решении уравнений модели с использованием ЭВМ. К моделям 1-ой группы можно отнести, например, модели Шумакова.
Модели регуляции сердечного выброса рассматривают основные свойства и характеристики сердца как насоса, сосудистой системы и контуров управления. Эти модели описываются, как правило, системами уравнений с сосредоточенными параметрами. Модели 2-ой группы можно разбить на разомкнутые и замкнутые. К разомкнутым моделям можно отнести модели Амосова с соавт., Григоряна. Наибольший интерес среди замкнутых моделей представляют модели Топам и Уорнера, Пикеринга с соавт., Гродинза с соавт., Джейнса. и Карсона, Палеца, Бенекена, Меллера, Гайтона, а также модели Шумакова с соавт. применительно к задачам искусственного и вспомогательного кровообращения.
С помощью моделирования велись многочисленные исследования реакции сердечно-сосудистой системы на физическую нагрузку. Модели системы кровообращения использовались при изучении различных патологических состояний, таких, как сердечная недостаточность, гипоксия, гипертоническая болезнь, блокада барорецепторов, изменение объема циркулирующей крови в системе кровообращения и т.п. Известны модели малого круга кровообращения (Палец и Бушная, Хьюмен). Математическая модель шестикамерного сердца предназначена для исследования динамики взаимодействия камер сердца, включая ушки предсердия.
Модели системы кровообращения успешно применяются для определения (идентификации) параметров системы по измерениям входа и выхода.
Рассмотрим класс моделей, для которых основой для разработки служит модель, предложенная академиком АМН Шумаковым В.И. и д. м. н., профессором Иткиным Г.П., описание модели приведено с их согласия. Главной особенностью данного класса моделей является то, что они позволяют изучать (моделировать) колебательные (в частности, периодические) процессы в системе кровообращения, в отличие от моделей усредненных характеристик. Эти модели являются самонастраивающимися (гомеостатическими), что отражает важнейшие свойства системы кровообращения.
Система кровообращения представляется динамической системой класса ДУ по классификации Неймарка:
![]() (1)
(1)
где i=1,2,. .,n (n-порядоксистемы),
j=l,2...,l (l-число различных описаний системы),
A1 ,... Ar - параметры, r-размерность пространства параметров,
Xi j - некоторые нелинейные функции, описывающие систему кровообращения на различных фазах.
Переход от описания р-й системой к описанию q-й системой (p,q 1,2,...,l}) уравнений (1) происходит при выполнении равенств:
Spq (xp 1 ,... xp n ,t,k1 ,...,k m ) = 0, (2)
где t - время, k1 ,..., km - переходные параметры,
m - размерность пространства переходных параметров.
В момент tpq перехода от описания р-й системой к описанию q-й системой (р-q-переход) значения новых переменных xq 1 ,...,xq n выражаются через значения старых переменных xp 1 ,...,xp n согласно уравнений скользящих движений:
![]() (3)
(3)
где i=1,2,. .,n s1 ,. .,ss - параметры скольжения.
Заметим, что рассматриваемая динамическая система неавтономна, поскольку в условия перехода (2) явно входит переменная t. Содержательное описание моделей будет дано в гл.1. Там же - приведены результаты цифрового моделирования, которые показали хорошее согласие с физиологическими данными.
Существование периодического движения динамической системы доказывается либо экспериментально численным моделированием на ЭВМ, либо аналитически, в зависимости от вида функций Xj i , Spq , Yi pq . В случае, если эти функции нелинейны, аналитическое решение вопроса о существовании периодических движений затруднительно.
Анализ устойчивости стационарных движений динамической системы позволяет установить факт реальности модели, поскольку реальная система кровообращения имеет стационарные устойчивые движения и из экспериментов известны характер и диапазоны их устойчивости. Кроме того, исследование устойчивости необходимо при анализе систем управления в аппаратах искусственного или вспомогательного кровообращения, при исследовании режимов внутриаортальной контрпульсации и т.д. Устойчивость изолированного стационарного движения динамической системы понимается в смысле Ляпунова, ее исследование аналитическими методами в общем случае уравнений (1) - (3) затруднительно.
В процессе идентификации системы координат измерению доступен вектор
y* ( t) = j ( A* , х* ( t)), (4)
зависящий от неизвестных параметров. Задача идентификации параметров системы кровообращения по измерениям (4), снимаемым с реального организма, ставится как задача определения параметров А модели (1) - (3) (а иногда дополнительно еще и параметров К и S), дающих наименьшее расстояние между y* (t) и соответствующими переменными
y ( t) = j ( A, x ( t)). (5)
При этом считается, что структура модели и объекта совпадают. Идентификация параметров проводилась различными методами: методом адаптивной идентификации, предложенным А.А. Красовским, методом прямого поиска, градиентными методами, методом наименьших квадратов по приспособленному базису и другими.
Требование идентичности, как правило, является глобальным и не исчерпывается идентичностью в одном заданном режиме (решение системы с фиксированными начальными условиями и параметрами). Проведенными машинными экспериментами было показано, что в системе (1) - (3) существуют режимы с неоднозначной идентификацией никоторых параметров. Поэтому перед проведением идентификации необходимо решить задачу идентифицируемости динамической системы в заданном режиме с заданной системой измерений (4), (5) либо задачу выбора системы измерений, на которых идентификация была бы идентификацией в целом.
Пусть Y - множество графиков y (t) вектор-функций (5), G - множество начальных условий для (1) в координатном n-мерном пространстве R n , A - множество параметров А. Для анализа наблюдаемости в отдельных режимах, глобальной (полной) наблюдаемости и идентифицируемости системы (1) - (5) разработаны методы и алгоритмы проверки биективности отображений Y ->G , Y ->A с помощью расчета ранга специально организованных матриц. [7]
В некоторых моделях обоих классов основное внимание обращается на свойство артериального русла преобразовывать входное прерывистое течение в более равномерное течение. Простейшей из таких моделей может служить модель "упругой камеры", в которой предполагается, что все флуктуации давления в артериях происходят синхронно. Эта модель, первоначально предложенная для определения ударного объема, модифицировалась много раз и недавно нашла новое применение при моделировании замкнутой сосудистой системы. Однако для исследования детального поведения самой артериальной системы упругая камера не пригодна, так как она не описывает распространение волн. Существенный недостаток модели упругой камеры привел к построению других моделей, в которых основное внимание уделялось трансмиссионным явлениям. Эти модели, также принадлежащие обоим классам, вначале были очень просты и состояли из однородных трубок с отражением на наружных концах. В своей основе модель упругой камеры и модель трубки считались взаимно исключающими.
Модель артериального древа человека с распределенными свойствами была разработана и сконструирована Ноордерграафом. В этой модели была использована пассивная электрическая аналогия, основанная на сходстве между уравнениями, описывающими распространения тока вдоль трансмиссионной линии, с одной стороны, и упрощенными уравнениями движения крови для течения в коротком сегменте артерии - с другой.
Впоследствии для исследования артериальной системы были построены и изучены несколько моделей с распределенными свойствами, имевших различную степень детализации. Де Патер и Ван-ден-Берг развили пассивную электрическую модель замкнутой системы кровообращения человека, применяя давление на конечные сегменты; по степени приближения к реальности их модель близка к модели, введенной Ноордеграафом.
Эти авторы ввели в свою модель теорию пульсирующих течений, используя в расчетах элементов, представляющих вязкость и инерцию крови, поправочные члены, основанные на приближении низких частот. Для более высоких частот (больше чем 3 Гц) низкочастотное приближение дает заметную разницу по сравнению с высокочастотным, особенно для артерий, отличных от аорты. В модели Де Патера абсолютное значение входного импеданса как функция частоты также колеблется с большей частотой, чем соответствующая частота у человека.
В этих работах была разработана модель с распределенными параметрами, в которой были использованы операционные усилители вместо пассивной электрической цепи. Этот Подход имеет то преимущество, что обладает большей гибкостью, однако возможность описания свойств, меняющихся вдоль артериального древа, ограничена количеством необходимых операционных единиц.
Расширенную математическую модель развили Тейлор, а также Эттингер. Чтобы воспроизвести артериальную систему, Тейлор описал случайно ветвящуюся модель (т.е. длина сосудов принималась случайно распределенной). Согласно этой модели, артериальное древо состоит из системы коротких однородных трубок, причем каждая трубка рассматривается как трансмиссионная линия. Было показано, что параметры этой системы трубок могут быть выбраны таким образом, что будет иметь место хорошее согласование с результатами реальных изменений по распространению волн и входному импедансу. На этой модели было выяснено, что по мере продвижения к периферии значение модуля упругости Юнга для стенок должно увеличиться (это условно названо "упругим сужением"). Хотя реальное артериальное древо организма не есть случайно ветвящаяся система, данная модель подчеркивает изобилие ветвлений.
Путем применения специальной техники сосудистое древо организма собаки было запрограммировано на ЭВМ Эттингером, Анне и их сотрудниками. Они использовали теорию пульсирующих течений, однако в противоположность модели Тейлора не ограничивались предположением, что толщина стенки мала по сравнению с радиусом. Модель Эттингера учитывает как геометрическое сужение сосудов, так и "упругое сужение". Эти авторы изучали, в частности, влияние степени агрегирования модели, а также влияние примененной ими теории пульсирующих течений на входной импеданс.
В исходной модели были сделаны противоречивые предположения при расчеты вязких и инерционных элементов в продольном импедансе. В новой модели такие противоречия утрачены путем пересчета продольного импеданса с использованием теории пульсирующих течений для коротких сегментов артерий, разработанной Витцигом и Уомерсли и развитой Ягером, которые учли динамику стенки и устранили предположение о тонкой стенке. Также в этой модели было учтено, что для теоретического изучения зависимости от расхода можно использовать пассивную электрическую аналогию.
Другой необходимой модификацией данной модели было использование симметричной (П-образной) сети вместо несимметричной (┐-образной) формы. Это привело к тому, что уменьшились ошибки, вводимые разбиением на конечные сегменты. Было так же установлено влияние "упругого сужения", то есть увеличения модуля упругости Юнга по направлению к периферии. В исходной модели не было возможности изменять локальные параметры; в заново сконструированной модели сделаны приспособления, допускающие ступенчатые изменения локального радиуса и упругости стенки. Демпфирование в стенке и нелинейные свойства стенки в модели не учитывались, хотя демпфирование можно учесть количественно в пассивной сети. [4]
Конструкция нового электрического аналога, основанного на теории пульсирующих течений.
На основе уравнений Навье-Стокса, уравнения неразрывности для движения жидкости, уравнения движения стенки сосуда и закона Гука для упрощенного материала можно вывести математические выражения для продольного и трансверсального импедансов сегмента артерии.
Распределение расхода по каждой из основных артерий пропорционально площади их поперечного сечения. При расчете нормальных региональных периферических сопротивлений предполагается, что среднее давление непосредственно перед периферическим сопротивлением составляет 100 мм рт. ст., и периферическое сопротивление получалось делением среднего давления на средний расход.
Левый желудочек рассматривается как граничное условие. Он представляется как волнопродуктор, так что в нем могут быть генерированы любые желаемые характеристики давления или любые характеристики начального течения. Когда желудочек рассматривается как источник давления, давление подается в модель через электрическую сеть, имитирующую аортальный клапан.
Так как аналог линеен, волнопродуктор может быть заменен синусоидальным осциллятором переменной частоты, позволяющим каждую гармонику рассматривать независимо и поэтому избежать необходимости анализа с помощью рядов Фурье.
Физиологические данные
Радиусы, которые были затабулированы Ноордеграафом при конструировании исходной модели, относились к субъекту роста 175 см и веса 75 кг. Большинство этих радиусов согласуются с данными, опубликованными позднее. Исключение представляют радиусы нижней брюшной аорты и бедренной артерии. Радиусы, в особенности радиусы аорты и крупных сосудов, имеют большое значение для получения модели, поведение которой близко к реальному.
Значения толщины стенки опубликованы Ноордерграафом. Следует заметить, что толщина стенки составляет приблизительно 10% внутреннего радиуса крупных сосудов и 25% - для мелких сосудов.
Общая длина моделируемых артерий составляет 720 см.
Полагается, что вязкость крови равна 3*10-2 пуаз и плотность крови составляет 1,05 г/см3 .
Модуль упругости Юнга был сначала принят равным 4*106 г*с-1 *сек-2 .
Конструкция модели.
Требования, предъявляемые к точности. Продольный импеданс. По радиусу отдельного сегмента в можно рассчитать число сопротивлений и индуктивностей, а корректирующей сети для этого сегмента в зависимости от точности, необходимой для самых высоких из интересующих нас частот (15 Гц). Испытания были проведены в широкой области частот.
Трансверсальный импеданс, т.е. значение емкости, реализовывался с погрешностью в пределах 3%.
Исходя из задаваемой степени точности для продольного и трансверсального импедансов индивидуальных сегментов, были определены допуски для характерных элементов, с помощью которых реализуются эти импедансы. Для этого использовались сердечники высокой магнитной проницаемостью, так как они позволяют сконструировать почти чистую индуктивность, которая необходима в корректирующей сети.
Сопротивления, меньшие 5 Ом, были выполнены из специальной проволоки, другие сопротивления и емкости делались из деталей, имеющихся в продаже.
Каждый сегмент был смонтирован в отдельной алюминиевой коробке, и все эти коробки были смонтированы на стойках (всего три стойки). Периферические сопротивления, представленные потенциометрами, устанавливались внутри коробок каждого концевого сегмента. В каждом сегменте записывались показания расхода (тока) посредством включения измеряющего прибора в отдельные доступные места проводки.
После соединения всех элементов измерялся продольный импеданс в широкой области частот. Эти измеренные значения сравнивались с ожидаемыми значениями импеданса, которые подсчитывались непосредственно с использованием таблиц, данных Уомерсли. Проверялся также трансверсальный импеданс. В некоторых случаях указанные импедансы необходимо было регулировать, чтобы учесть емкость проводки.
Ошибка, вводимая агрегированием, может быть уменьшена, особенно для высоких частот, посредством использования симметричной сети (П) вместо несимметричной (┐). Характеристический импеданс Z0 ┐и волновое число γ┐ однородной линии передачи, агрегированной в конечные сегменты, могут быть выражены как функции характеристического импеданса Z0 и волнового числа γ реальной линии передачи (с бесконечно короткими сегментами). Возникающая за счет агрегирования ошибка в значении Z0 ┐имеет порядок γΔz/2, а в значении γ┐ - порядок (γΔz/2) 2 , где Δz - длина сегмента. Для симметричной сети (П) нами найдено, что ошибка как в Z0П , так и в γП имеет порядок (γΔz/2) 2 . В нашей модели величина γΔz выбиралась так, чтобы она была приблизительно постоянна по всей системе, т.е. длина сегментов аорты меньше, чем периферических сосудов. Ошибки из-за агрегирования увеличиваются с частотой. При частоте 15 Гц γΔz величина приблизительно равна 0,5, и ясно, что это дает ошибку в величине Z0 ┐около 25%, а в величине Z0П - только около 6%; следовательно, симметричная сеть является лучшей аппроксимацией по сравнению с несимметрично сетью.
Оценка модели
Симметричная сеть была введена как следующее улучшение, и в качестве примеры был приведен входной импеданс артериального древа организма в целом. Отсюда модно заключить, что в отношении входного импеданса, который "ощущается" левым желудочком, длина сегментов достаточно мала для интересующей нас области частот.
Недостаточное количество данных не позволяет приписать основные локальные значения модуля Юнга различным артериям, представленным в исходной модели. Поэтому в качестве рабочей гипотезы было принято, что среднее значение модуля Юнга можно использовать для всех артерий древа.
Измерения Бергеля, Лиройда и Тейлора показали, что модуль Юнга для различных артерий различен. К тому же модуль Юнга зависит от частоты и величины механических напряжений.
Поводя итог, модно сказать, что с точки зрения влияния на входной импеданс улучшения весьма малы. По-видимому, входной импеданс системы в целом совершенно нечувствителен к рукавному эффекту, симметричной сети или даже к упругому сужению. Также он не зависит практически от периферического сопротивления. [4]
В качестве примера вполне работоспособной модели второго класса с разбиением, близким к оптимальному, можно рассмотреть модель кровообращения, представленную на рисунке 1.

Рис.1. Блок-схема модели кровообращения
Обозначения на рисунке:
А - артерии, В - вены, К - капилляры, Ж - желудочек, П - предсердие, КС - каротидные синусы, ЯВ - яремные вены, ДА - дуга аорты, НА - нисуолящая аорта, ПА - подключичная артерия, ВВ - верхняя полая вена, ГВ и БВ - грудная и брюшная нижние полые вены.
Насосная функция сердца описывается уравнением:

Здесь Q- объемный кровоток на выходе желудочка
F- частота сердечных сокращений
K- сократительная способность сердца
C- диастолическая растяжимость желудочка
Pv - венозное давление на входе сердца
U- ненапряженный объем желудочка при P=0
Vo - свободный член статической аппроксимации Q=Q (Pv ).
Экспоненциальные члены описывают динамику процесса с учетом гидравлического сопротивления атриовентрикулярных клапанов и длительности диастолы ![]() , причем
, причем
![]()
где a и b - константы. Объем крови Vi =Vi (t) для i-го участка системы задается уравнением баланса
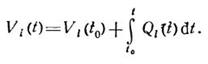
Здесь Qi - алгебраическая сумма по j объемных скоростей кровообмена qij между i-м участком и всеми остальными, причем qij ≡0, если j-ый участок непосредственно не сообщается с i-ым. В противном случае принимается, что
![]()
где Pi - суммарное давление крови на i-ом участке,
Ri - сопротивление кровотоку на этом участке.
В модели учитывается, что в некоторых периферических венах при падении давления сечение приобретает эллиптическую форму. Для этих сосудов принималось:
![]()
А для сосудов верхней половины тела:
![]()
Здесь ![]() - сопротивление сосуда в условиях, когда его объем равен Ui- ненапряженному объему;
- сопротивление сосуда в условиях, когда его объем равен Ui- ненапряженному объему;
![]() - сопротивление сосуда при горизонтальном положении тела, когда объем сосуда равен
- сопротивление сосуда при горизонтальном положении тела, когда объем сосуда равен ![]() .
.
Зависимость трансмурального давления ![]() (давления, обусловленного упругостью сосудистой стенки) от рассматриваемых переменных имеет вид:
(давления, обусловленного упругостью сосудистой стенки) от рассматриваемых переменных имеет вид:
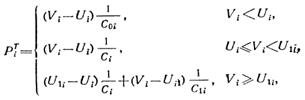
где ![]() - объемная податливость сосудов соответственно в области отрицательного, низкого положительного и высоко положительного давлений;
- объемная податливость сосудов соответственно в области отрицательного, низкого положительного и высоко положительного давлений;
![]() - параметр аппроксимации.
- параметр аппроксимации.
Суммарное давление в i-ом сосуде равно:
![]()
Здесь ![]() - гидростатическое давление, пропорциональное величине действующей перегрузки и отсчитываемое от выбранного нулевого уровня (обычно от уровня нижней точки тела или уровня сердца);
- гидростатическое давление, пропорциональное величине действующей перегрузки и отсчитываемое от выбранного нулевого уровня (обычно от уровня нижней точки тела или уровня сердца);
![]() - давление в тканях, окружающих i-ый участок сосудистого русла:
- давление в тканях, окружающих i-ый участок сосудистого русла:
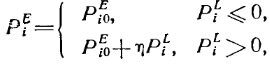
причем ![]() - избыточное давление на поверхности тела в зоне i-го элемента модели;
- избыточное давление на поверхности тела в зоне i-го элемента модели;
![]() - внесосудистое давление в тканях в условиях физиологической нормы
- внесосудистое давление в тканях в условиях физиологической нормы
ŋ - коэффициент передачи давления, ŋ ≤1.
Эти уравнения полностью описывают биомеханическую модель кровообращения в условиях измененной весомости и перепадов давления по телу. Для учета физиологических компенсаторных реакций в модель дополнительно вводится контур автоматического регулирования давлений крови в зонах аорты и каротидных синусов. В качестве регулируемых параметров приняты частота и сила сердечных сокращений, а также сопротивление, податливость и ненапряженный объем участков сосудистого русла. Отклонение давлений в контролируемых зонах от исходных "нормальных" значений (давления в покое в позе "лежа") приводит к включению схемы пропорционального регулирования вышеперечисленных параметров, причем для каждого из них справедливо уравнение
![]()
где Δα - отклонение регулируемого параметра от исходного значения
kα - коэффициент усиления;
Тα - постоянная времени для этого параметра.
Пример использования описанной модели кровообращения для исследования реакций организма на воздействие повышенной весомости приведен на рисунке 2:
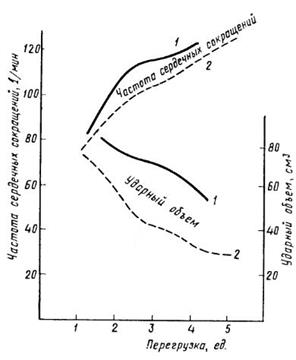
Рис.2. Изменение параметров кровообращения при повышенной весомости. 1 - эксперимент, 2 - расчет.
Видно, что расчетные кривые хорошо отражают качественное изменение физиологических параметров. Практически это означает, что рассмотренный метод расчетной оценки может быть использован для проведения модельных экспериментов по исследованию влияния параметров перегрузки (значение, длительность, скорость нарастания, направление относительно тела человека) и эффективности средств защиты (изменения положения тела, величины, локализации, режима приложения избыточного давления к различным участкам тела). При этом можно ожидать, что полученные результаты будут достаточно надежными, по крайней мере в качественном плане ("лучше","хуже","больше на 30-40%" и т.д.).
Еще более интересной представляется возможность количественного прогнозирования функциональной прочности организма в условиях повышенной весомости, в частности при использовании различных средств компенсации. Для решения этой задачи рассмотренная модель кровообращения нуждается в двух модификациях. Первая, более простая, состоит в уточнении некоторых аналитических соотношений (прежде всего регуляторных) и числовых параметров модели, вторая - в выборе критерия функциональной прочности, учитывающего состояние сознания и уровень работоспособности. Критичным в этом плане является кровоснабжение головного мозга, так что искомый критерий К будет функцией одного или нескольких показателей мозгового кровотока (например, давления крови в тканях мозга, кровенаполнения и/или объемного кровотока).
Пусть в i-ом модельном эксперименте значение величины К (t) упало до уровня Ki * к моменту времени, когда в реальных условиях возникли нарушения сознания и недопустимое снижение работоспособности оператора. Среднее значение K*, полученное при моделировании ряда экспериментальных режимов, даст искомый критерий. Если теперь при модельном анализе нового режима воздействия окажется, что расчетное значение К (t) во всех случаях превышает критическое K*, то можно с некоторой вероятностью считать рассматриваемое воздействие переносимым, а используемые средства компенсации - эффективными.
Использование такого качественного критерия типа "допустимого-недопустимого" представляет определенный практический интерес, но более перспективным было бы использование вероятностного прогнозирования функциональной прочности в условиях повышенной весомости с учетом результатов статического моделирования переносимости, описанного выше.
Следует помнить, что описанная модель может оказаться слишком грубым инструментом для столь подробного количественного исследования. Выявление вероятностных зависимостей между параметрами мозгового кровообращения и состоянием сознания целесообразно проводить, используя более подробное описание особенностей сосудистого русла и механизмов регуляции, прежде всего мозгового кровообращения. [1]
Упрощенная модель системы кровообращения
В упрощенной модели системы кровообращения каждая цепь (как малого, так и большого круга кровообращения) имеет одинаковую структуру и состоит из линейных объемных податливостей (СА для артерии и Сv для вены), связанных на периферии через линейное сопротивление, описываемое уравнением Пуазейля.
Для людей молодого возраста (16-39 лет) объемная податливость CAS =1 мл/ (мм рт. ст). Объемную податливость вен большого круга можно оценить, если принять, что при кратковременной остановке сердца среднее системное давление равно примерно 10 мм рт. ст., а весь объем циркулирующей крови (5 литров) сосредоточен в венах большого круга. Отсюда CAS ≈500 мл/ (мм рт. ст).
Оценить величину периферического сопротивления (RS ) большого круга можно, предположив, что средние значения давлений в артериальном и венозном резервуарах равны соответственно 100 и 20 мм рт. ст.; средняя величина минутного кровообращения 5 л/мин.
Отсюда RS = 20 (мм рт. ст) / (л/мин).
В упрощенной гидравлической модели системы кровообращения (рис.3) один механический насос (левый) перекачивает кровь из легочной вены в артерию большого круга со скоростью QL , а второй (правый) перекачивает кровь из вены большого круга в легочную артерию со скоростью QR . Индексы A и V относятся, соответственно, к артерии и вене, а P и S- к цепям малого и большого кругов. Система содержит фиксированный объем крови B, распределенный между четырьмя резервуарами, причем предполагается, что объем насосов и связывающих их трубок пренебрежительно мал.
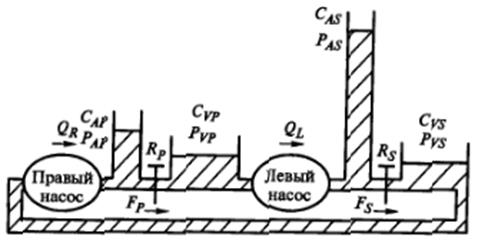
Рис.3. Гидравлический аналог системы кровообращения.
Весьма просто записать систему уравнений, описывающих работу этого аналога. Сначала сформулируем уравнение неразрывности для каждого из четырех резервуаров. Так скорость изменения объема крови в артерии большого круга BAS равна разности между скоростью притока QL и скоростью оттока FS . Но поскольку податливость артерии CAS равна, по определению, отношению объема к давлению (т.е. CAS =BAS /PAS ), то очевидно, что BAS = CAS PAS .
Следовательно, имеем CAS PAS = QL - FS .
Для каждого из оставшихся трех резервуаров могут быть записаны аналогичные уравнения:
CVS BVS =-QR +FS ; (1)
CAP PAP =QR -FP ; (2)
CVP PVP =- QL + FP . (3)
Далее запишем уравнения Пуазейля:
FS = (PAS - PVS ) / RS; (4)
FP = (PAP - PVP ) / RP ; (5)
Подставляя уравнения (4) - (5) в уравнения (1) - (3) и приводя их к общему знаменателю, получим:
RS CAS PAS + (PAS - PVS ) = RS QL ; (6)
RS CVS PVS - ( PAS - PVS ) = - RS QR ; (7)
RP CVS PVP + (PAP - PVP ) = RP QR ; (8)
RP CVP PVP - ( PAP - PVP ) = - RP QL . (9)
Описанная упрощенная структурная схема системы кровообращения является основой многих математических и физических моделей, используемых для исследования регуляции кровообращения, в клинической практике для идентификации индивидуальных (для конкретного пациента) параметров насосной функции сердца, центрального и периферического кровообращения, в лабораторных исследованиях конструкций протезов сосудов, искусственных клапанов и желудочков сердца.
Количественной характеристикой течения крови является линейная скорость кровотока, т.е. скорость перемещения малого объема крови, размер которого намного меньше сосуда. [8]
Заключение
Исследование структуры системы кровообращения и механических процессов, происходящих в отдельных ее элементах, дает возможность строить различные математические модели функционирования системы в целом, подобные приведенным ранее, и решать с помощью этих моделей некоторые теоретические и практические задачи. Например, предсказывать реакцию системы на перегрузки или падение внешнего давления, анализировать гипотезы о механизмах регуляции, изучать распространение метаболитов, кислорода, лекарственных веществ и индикаторов в организме и т.д.
Термин "моделирование" означает здесь в сущности решение достаточно сложной системы уравнений ЭВМ. Для проведения такого исследования необходимо знать эти уравнения, граничные и начальные условия и числовые значения определяющих параметров.
Физическое моделирование системы кровообращения, к которому, кроме экспериментов на гидравлических устройствах, нужно отнести еще и опыты, поставленные на животных одного вида с целью применить результаты к животным других видов, выдвигает ряд совершенно иных проблем, главная из которых - установление взаимосвязи между параметрами модели и реального объекта.
Поскольку деятельность сердечно-сосудистой сиcтемы и деятельность других физиологических систем тесно связаны друг с другом, то может быть поставлен вопрос об основных универсальных принципах этой связи. Ряд исследователей склоняется к мысли, что эволюция развития животных могла привести к некоторой оптимальной (в термодинамическом смысле) организации физиологических систем, такой, что, например, связь между процессами кроветворения и, дыхания и кровообращения определяется условием оптимального снабжения тканей кислородом. Постулируя оптимальность такого рода, можно провести расчеты некоторых заранее неочевидных соотношений между параметрами системы и сопоставить затем результаты с опытными данными для проверки исходной гипотезы. [5,6]
Список использованной литературы
1. И.Ф. Образцов, И.С. Адамович, А.С. Барер. "Проблемы прочности в биомеханике", издательство "Высшая школа", Москва 1988 год
2. П.И. Бегун, П.Н. Афонин. "Моделирование в биомеханике", издательство "Высшая школа", Москва 2004 год
3. Сборник переводов под редакцией С.А. Регирера "Гидродинамика кровообращения" издательство "Мир", Москва 1971 год
4. Н. Вестергоф, Ф. Босман, К. Дж. Де Вриз, А Ноордерграаф. Журнал по биомеханике "Аналитическое исследование артериальной системы человека". 1969 год.
5. М.А. Ханин, И.Б. Бухаров. К феноменологической теории функциональных параметров регулирования системы транспорта кислорода, 1970 год
6. П. Розен. "Принцип оптимальности в биологии". Лондон, 1967 год
7. Ю.В. Солодянников. "Элементы математического моделирования и идентификация системы кровообращения". Издательство "Самарский университет", Самара 1994 год
8. В.Б. Парашин, Г.П. Иткин. "Биомеханика кровообращения". Издательство МГТУ имени Н.Э. Баумана, Москва 2005 год