| Скачать .docx | Скачать .pdf |
Реферат: Как гены человека наносят на карту.
Красноярский Государственный
Педагогический Университет
Реферат
Тема : Как гены человека наносят на карту
работу выполнил:
студент группы 40
факультета информатики
Шишканов Д.В.
проверил:
Никольский
Красноярск 2000г.
Введение
Генетика человека как фундаментальная, так и прикладная наука. Как фундаментальная наука - это область генетики, которая изучает законы наследственности и изменчивости у самых интересных организмов - человеческих существ. Научные результаты, полученные при этом, ценны для нас не только в теоретическом плане. Вот почему генетика - это также и прикладная наука. Важность ее для благополучия человечества очень велика, успехи, достигнутые в этой области, приносят ученым большую радость, чем новые сведения, полученные в чисто теоретических или чисто прикладных исследованиях.
По данным Всемирной организации здравоохранения, около 2,5% новорожденных появляются на свет с различными пороками развития. При этом 1,5-2% из них обусловлены преимущественно неблагоприятными внешними (экзогенными) факторами, а остальные имеют преимущественно генетическую природу. Генетические факторы пороков развития отражают так называемый общий генетический груз популяции, который проявляется более чем у 5% населения планеты. Примерно 1% генетического груза приходится на генные мутации, 0,5% - на хромосомные мутации, около 3-3,5% соответствует болезням с выраженным наследственным компонентом (диабет, атеросклероз, ишемическая болезнь сердца, некоторые опухоли и т.д.). Если к этому добавить, что около 40-50% ранней младенческой смертности и инвалидности с детства обусловлены наследственными факторами и примерно 30% коек в детских стационарах заняты детьми с наследственной патологией, становится понятной безусловная необходимость правильной и рационально организованной ранней диагностики врожденных и наследственных болезней (пренатальной диагностики). Знания в области генетики позволили бы не только установить диагноз еще до рождения, но и предотвратить появление на свет детей с тяжелыми, неисправимыми пороками развития, с социально значимыми смертельными генными и хромосомными болезнями.
Число генных болезней, доступных молекулярной диагностике, уже превышает 1000 и продолжает быстро увеличиваться. Созданы и постоянно совершенствуются все новые эффективные и достаточно универсальные методы ДНК-диагностики, такие, как метод полимеразной цепной реакции (ПЦР), автор которой – американский ученый Кэй Муллис отмечен Нобелевской премией 1994 года, метод гибридизации, увековечивший имя его создателя Эд. Саузерна (1975 год), и методы ДНК-секвенирования (анализ первичной последовательности нуклеотидов в цепочке ДНК), разработанные П. Сэнджером.
Несколько лет назад начались исследования по международной программе "Геном человека", объединившей усилия ученых многих стран. Конечная цель ее – создать подробную карту человеческого генома, то есть полного набора его генов. А цель предлагаемого реферата гораздо более скромная: пробившись сквозь завесу заумных терминов (в каковом отношении генетика – дисциплина неудобоваримая даже для самих генетиков), ввести читателя в курс одного из величайших научных проектов века.
География генома
До сих пор возможности науки позволяли составлять разве что генетические карты совсем простеньких организмов, вроде кишечной палочки. Если всю последовательность ее генов, составляющих единственную замкнутую хромосому, распечатать на бумаге в столбик мелким шрифтом, присвоив каждому гену короткое имя из трех-четырех букв, получится книжица страниц в 300 обычного формата. А если так же поступить с человеческим геномом – итоговый труд займет 200 томов по 1000 страниц каждый.
 Ныне эта необъятная "библиотека" напоминает скорее свалку книг: большинство листов не заполнено, остальные перепутаны, и вообще далеко не всегда ясно, какой том за каким идет. Известно, что геном человека насчитывает около 80000 генов, состоящих в сумме примерно из 3 млрд. пар нуклеотидов (так называется мономер двойной спирали ДНК, подобно тому как аминокислота – мономер белковой молекулы). Локализовано же всего 7000 генов – меньше 10%. Для некоторых районов генома, представляющих особый интерес, составлены довольно детальные карты, для остальных – весьма приблизительные либо вовсе никаких.
Ныне эта необъятная "библиотека" напоминает скорее свалку книг: большинство листов не заполнено, остальные перепутаны, и вообще далеко не всегда ясно, какой том за каким идет. Известно, что геном человека насчитывает около 80000 генов, состоящих в сумме примерно из 3 млрд. пар нуклеотидов (так называется мономер двойной спирали ДНК, подобно тому как аминокислота – мономер белковой молекулы). Локализовано же всего 7000 генов – меньше 10%. Для некоторых районов генома, представляющих особый интерес, составлены довольно детальные карты, для остальных – весьма приблизительные либо вовсе никаких.
Карты генома, как и географические, можно строить в разном масштабе, с различным уровнем разрешения – последний зависит от точности метода анализа. Существует две разновидности карт генома – собственно генетические, получаемые косвенными методами, и физические – результат прямого исследования молекулы ДНК. Максимально возможная степень детализации – с точностью до пары нуклеотидов (далее п.н.). Иными словами, самая крупномасштабная карта – полная последовательность нуклеотидов с указанием, где кончается один ген и начинается следующий. Но это предел мечтаний, и пока до него далеко. А то, чем мы сегодня располагаем, - главным образом мелкомасштабные карты всех 23 пар человеческих хромосом с расстоянием между отдельными маркерами – мельчайшими "различимыми на местности объектами" – 7-10 млн. п.н.
Начнем с карт, составляемых при помощи косвенных методов изучения генома.
Карты генетического сцепления
Прежде всего заметим, что человеческая ДНК состоит, строго говоря, не только из генов. Ген, или экзон, - это экспрессируемый участок молекулы ДНК, иначе говоря, ее отрезок, на котором, как на станке, "штампуются" молекулы того или иного белка. Но подавляющее большинство нуклеотидных последовательностей в ДНК – интроны, не кодирующие ничего. Не всегда ясно, зачем они нужны и что делают, но – явно нужны и делают, иначе бы их не было.
Карта генетического сцепления составляется так. Сначала нужно выбрать маркеры – какие-нибудь признаки организма, о которых точно известно, что они наследственные, а не "благоприобретенные". Правда, признак годится на роль маркера, лишь если по нему имеются различия между индивидами и если эти различия легко выявить. Скажем, цвет глаз, или группа крови, или предрасположенность к некоей болезни.
После того как маркеры выбраны, начинается анализ их наследования. У генов есть одно любопытное свойство – они могут рекомбинировать, т.е. перераспределяться. Либо в процессе развития сперматозоидов и яйцеклеток цепочка ДНК случайным образом разрывается и воссоединяется в разных местах, либо просто две хромосомы, составляющие пару (гомологичные), обмениваются соответственными участками. В обоих случаях получается новое сочетание признаков – те, что обычно наследуются совместно, разделяются.
Так вот, известна закономерность: чем ближе друг к дружке расположены два гена на хромосоме, тем труднее им "распрощаться" при рекомбинации – один "тянет" за собой другой. На этом и основано построение карт сцепления. Чем реже происходит рекомбинация между данными двумя признаками-маркерами, тем меньше расстояние между генами, их кодирующими.
Правда, таким путем можно выяснить лишь взаимное расположение "действующих" геном (экзонов) – вернее, вычислить расстояние между ними на хромосоме по частоте рекомбинаций. Установлено, что если последняя равна 1%, дистанция между генами составляет примерно 1 млн. п.н., или 1 Мб (одну мегабазу – последнее слово и означает "миллион оснований", т.е. нуклеотидов). Одна мегабаза "на местности" соответствует 1 сМ на карте (одной сантиморганиде – название этой единице дали честь великого генетика Т.Х. Моргана).
Но аналогичным способом можно картировать и интроны. Для них маркерами обычно служат так называемые сайты узнавания. Дело в том, что существуют специальные ферменты, предназначенные для разрезания ДНК, - рестриктазы. Это белковые молекулы особого устройства. Грубо говоря, они попросту "шинкуют" ДНК, режут на отрезки, но не как попало, а в определенных местах. Всякая рестриктаза может опознать лишь одну стандартную последовательность из нескольких нуклеотидов. Последняя и становится сайтом узнавания для фермента. А уж как тот "покромсает" ДНК, зависит от того, сколь густо она "усеяна" сайтами узнавания. Молекулы рестриктазы химически связываются с ними и в этих местах рвут цепь ДНК.
Имеются сравнительно простые методы измерения длин участков, на которые порезала молекулу ДНК рестриктаза. Любое изменение сайта узнавания ведет к тому, что тот становится "невидимым" для фермента. А значит, ДНК разрезается в других местах и образуются иные по длине фрагменты.
Чем хорош метод картирования по генетическому сцеплению – его можно применять, не имея ни малейшего представления о структуре генов тех или иных признаков. Достаточно уверенности, что таковые гены есть, а дальнейшие мероприятия направлены на то, чтобы узнать, ГДЕ они, а не КАКИЕ они.
Недостатки метода – довольно низкая разрешающая способность (7-10 Мб) и высокая трудоемкость. Кроме того, ген на карте предстает не протяженным отрезком ДНК (каков он "на местности"), а точкой на линии, изображающей ее двойную цепь.
Наконец, к великому сожалению, человек – не дрозофила. Очень легко считать частоту рекомбинации маркеров, скрещивая мелких мушек тысячами и десятками тысяч. А с Homo sapiens такой способ по понятным причинам не годится, и о частоте рекомбинации приходится судить по статистическим данным – скажем, по заболеваемости таким-то наследственным недугом в стольких-то семьях за столько-то десятилетий (а то и веков). Кстати, именно генетическое картирование помогло найти точное расположение на хромосомах генов многих тяжелых наследственных болезней – муковисцидоза, серповидно-клеточной анемии, хореи Гентингтона, болезни Тея-Сакса, поликистоза почек, миотонической дистрофии и других.
Мелкомасштабные физические карты
К ним относят хромосомные и карты кДНК ("к" значит "кодирующей").
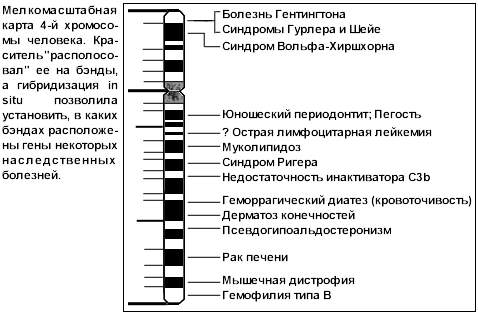
Хромосомное картирование довольно грубо, но имеет смысл, когда нужный ген держат, что называется, в руках: известна его структура, он химически выделен, но неизвестно, где он "сидит". Тогда хромосомы, извлеченные из ядра клетки во время ее деления (когда они толстые и хорошо различимы), обрабатывают особыми красителями, придающими им "полосатость": получаются так называемые бэнды – разноокрашенные участки хромосом. Искомый ген размножают в пробирке и при этом метят его копии, подменяя, например, водород тритием. За таким радиоактивным зондом очень удобно следить: если подмешать его к препарату хромосом и выдержать некоторое время, он химически свяжется с определенным бэндом определенной хромосомы, встав "на свое место" (это называется "гибридизация in situ", т.е. "на месте"). Так были картированы гены альбумина, коллагена, гормона роста и некоторые другие.
Средний размер бэнда – около 10 Мб: такова и точность хромосомной карты. Правда, позднейшее усовершенствование – гибридизация с флуоресцентной меткой (FISH – fluorescent in situ hybridization) – повысило разрешение до 5-2 Мб. Более того, разработан даже метод гибридизации меченых генов с хромосомами, извлеченными из ядра неделящейся клетки – и значит, де конденсированными, "развинченными", а не упакованными в компактные образования. В итоге удалось локализовать участки до 0,1 Мб.
 |
Карты кДНК отражают расположение экспрессирующихся нуклеотидных последовательностей. По-русски это означает следующее. Допустим, в клетке активно работает, производя белок, некий ген. Что за ген – неизвестно. Где он – тоже. Тогда пользуются тем обстоятельством, что при синтезе белка в клеточном ядре сначала "штампуются" молекулы мРНК – точные копии работающего гена ("м" – матричные). Сей промежуточный продукт можно выловить из клетки и размножить в пробирке, пометив тритием либо радиоактивным фосфором. А дальше все как при хромосомном картировании: зонд пристроился к участку N – значит, экспрессия шла здесь и, следовательно, здесь расположен ген, кодирующий данный белок.
Крупномасштабные карты генома
Их составляют по общему принципу: сначала кромсают ДНК на куски, разгоняют получившиеся фрагменты в электрическом поле (электрофорез) и затем гибридизируют с меченым зондом. В результате фрагменты упорядочиваются – воссоздается их исходная последовательность. Для этого используют разные методы поиска перекрывающихся участков.
В любом случае необходимо прежде всего получить фрагменты ДНК картируемого участка в больших количествах. ДНК размножают обычно двумя способами – клонированием и ПЦР.
КЛОНИРОВАНИЕ – по современным понятиям сравнительно примитивный метод. Последовательность действий такова: порезали рестриктазой изучаемый участок ДНК – вставили каждый ее отрезок в молекулу вектора (бактериальной, дрожжевой или другой кольцевой ДНК), разрезанную в одной точке той же рестриктазой: получилась рекомбинантная кольцевая ДНК с "чужой" вставкой. Такую смешанную ДНК "вселяют" в ядро клетки-хозяина (обычно бактерии), и та принимается делиться в культуре, благодаря рекомбинантная ДНК – и.о. ее генома – размножается практически до любого количества копий. Результат – набор клонов разных фрагментов картируемой ДНК, или, как его обычно называют, библиотека клонов.
ПОЛИМЕРАЗНАЯ ЦЕПНАЯ РЕАКЦИЯ (ПЦР) – лабораторный синтез фрагментов ДНК без клетки-хозяина. В пробирку к фрагменту, который надо размножить, "подсаживают":
а) фермент ДНК-полимеразу, который осуществляет воспроизведение ДНК в живых клетках;
б) стройматериал, т.е. отдельные нуклеотиды;
 |
в) прамеры – короткие цепочки нуклеотидов, соответствующие концам размножаемого фрагмента. Тут, как видите, слабое место метода: про упомянутый участок надо кое-что знать заранее – а именно структуру праймеров…
Затем пробирку нагревают – фрагмент от жары "расклеивается", разделяясь на две цепи; пробирку охлаждают – праймеры присоединяются к концам фрагмента и полимераза начинает свое дело. Чередуя нагревания и охлаждения, можно за полтора часа довести количество копий нужного участка ДНК до нескольких миллионов – в чем и состоит главное преимущество ПЦР перед клонированием. Но у нее есть два недостатка. Один уже упомянут – нужно знать праймеры "в лицо", иначе реакцию не удастся запустить. Второй – техническая невозможность копировать фрагменты длиннее 5-6 п.н.
После того как все фрагменты ДНК получены в достаточном количестве копий, их упорядочивают, для чего сперва разделяют электрофорезом, а затем химически связывают (гибридизуют) с меченым зондом, чтобы каждый фрагмент встал на свое место и, так сказать, просигналил о себе: вот он я!
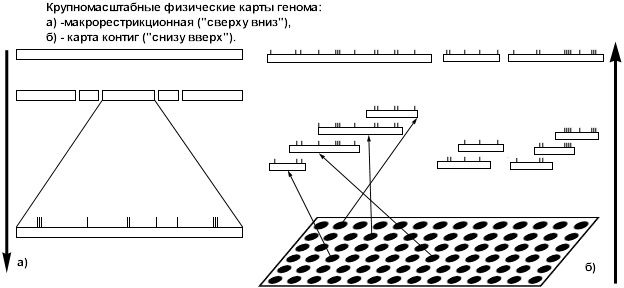
Крупномасштабные физические карты генома бывают двух типов. Первый – МАКРОРЕСТРИКЦИОННЫЕ (по принципу "сверху вниз"): ДНК режут редкощепящей рестриктазой на крупные куски, упорядочивают их, потом делят на более мелкие, которые тоже упорядочивают. Такая карта охватывает довольно большие участки генома – до 10 Мб – и не содержит пробелов. Но ее разрешение сравнительно невелико – от 1 Мб до 100 кб.
Гораздо выше точность у КАРТ КОНТИГ. Их строят по обратному принципу – "снизу вверх". Хромосому шинкуют на очень короткие фрагменты, размножают их и упорядочивают. Набор упорядоченных коротких фрагментов, покрывающих определенный участок хромосомы, - это и есть контига. А где сама она расположена на хромосоме, можно установить методом FISH.
Правда, карту контиг трудно расширить до крупных районов хромосомы, поскольку нельзя размножать большие фрагменты ДНК – ни клонированием, ни ПЦР. Хотя в последние годы достигнут серьезный успех: удалось создать гигантскую молекулу-вектор, в которую можно встроить участок человеческой ДНК размером до мегабазы. Этот вектор называется YAC – the yeast artificial chromosome, искусственная дрожжевая хромосома. До внедрения YAC в качестве векторов применялись в основном бактериальные плазмиды – крошечные колечки ДНК, несшие вставки чужеродного материала максимум в 20-40 кб. Смысл применения YAC – значительное уменьшение числа клонов, которые нужно упорядочивать.
Прогулка по хромосоме
Все описанные выше методы позволяют создавать либо приблизительные карты обширных регионов генома, либо подробные "топографические планы" мелких его участков. Как совместить то и другое – закартировать большой район, но детально?
Современная стратегия заполнения пробелов – прогулка по хромосоме. Ее начинают с какого-нибудь короткого участка, чья нуклеотидная последовательность уже расшифрована. По ней синтезируют праймер, гибридизируют его с первым попавшимся клоном из неупорядоченной геномной библиотеки, а затем "подключают к делу" полимеразу – она делает цепь, комплементарную данному клону. Затем эту цепь секвенируют, а ее хвостик используют в качестве праймера для следующего шага по хромосоме.
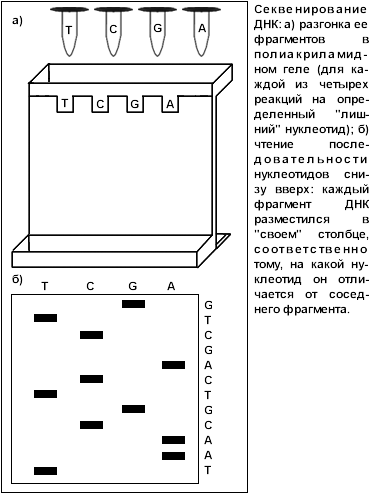
Вот и прозвучало слово "секвенирование". Так называется новейший, прославленный, подробнейший, точнейший… и, с позволения сказать, тягомотнейший метод картирования генома. Его сущность – полная расшифровка последовательности нуклеотидов. Чтобы в деталях объяснить, как она осуществляется, потребовалась бы двухчасовая лекция по молекулярной биологии. Посему в двух словах: из библиотеки клонов извлекают фрагмент ДНК, вновь клонируют, а получившиеся копии химически преобразуют в набор отрезков ДНК, различающихся по длине лишь на один нуклеотид (вот именно эту стадию практически невозможно описать общедоступным языком – настолько она сложна даже для генетика-профессионала). Затем упомянутые отрезки разделяются на гелевой пластинке в пульсирующем электромагнитном поле (пульс-форез). Последовательность нуклеотидов читают по фореграмме: каждый отрезок "уезжает" по гелевой пластинке настолько далеко, сколь велика его длина, и занимает место в одном из четырех столбцов – в зависимости от того, на какой нуклеотид (а их всего четыре типа) он длиннее соседнего.
 Хотя современные усовершенствования позволяют изучать одновременно до 40 клонов на одном геле, затраты времени и средств все равно огромны. Даже опытная рабочая группа на лучшем оборудовании секвенирует в год не более 100000 п.н. в год. Если принять стоимость анализа каждой пары оснований за доллар – весь геном человека может быть секвенирован за 3000 лет, и обойдется его изучение в 3 миллиарда долларов. Сумма по нынешним временам вполне приемлемая хотя бы на слух, но вот время… Сейчас, правда, развиваются технологии секвенирования второго поколения – высоковольтный капиллярный электрофорез, ионизационная резонансная спектроскопия. Они ускоряют процесс на порядок – стало быть, хватит трех веков (за те же деньги). Обнадеживает, но не слишком.
Хотя современные усовершенствования позволяют изучать одновременно до 40 клонов на одном геле, затраты времени и средств все равно огромны. Даже опытная рабочая группа на лучшем оборудовании секвенирует в год не более 100000 п.н. в год. Если принять стоимость анализа каждой пары оснований за доллар – весь геном человека может быть секвенирован за 3000 лет, и обойдется его изучение в 3 миллиарда долларов. Сумма по нынешним временам вполне приемлемая хотя бы на слух, но вот время… Сейчас, правда, развиваются технологии секвенирования второго поколения – высоковольтный капиллярный электрофорез, ионизационная резонансная спектроскопия. Они ускоряют процесс на порядок – стало быть, хватит трех веков (за те же деньги). Обнадеживает, но не слишком.
По всей видимости, программа "Геном человека" будет успешно выполнена лишь по технологиям третьего поколения, ныне существующих в зачаточном состоянии. К ним в частности, относится прямое чтение последовательности нуклеотидов с помощью сканирующей туннельной или атомной микроскопии. Сегодняшняя наука делает ставку именно на такие методы – иначе прогулка по человеческим хромосомам грозит затянуться на тысячелетия.
Заключение
И вот на глаза мне попалась журнальная заметка, датированная мартом 2000 года, о том, что расшифрована последовательность ДНК 22-й человеческой хромосомы. Это первая наиболее полная расшифровка целой структуры в генетическом аппарате человека и – 1/23 часть глобального проекта "Геном человека". Впечатляют масштабы коллективного авторства – 216 ученых из Великобритании, США, Японии, Канады и Швеции. Только эта хромосома содержит более 20 генов, изменения в которых приводят к известным заболеваниям человека, в частности (предположительно), и один из генов, обусловливающих шизофрению. Для полного раскрытия генома человека трудиться еще придется долго. Однако, по мнению руководителя геномного проекта Фрэнсиса Коллинза, нынешнее достижение можно уже сравнить с "расщеплением атома или полетом на Луну".
Жуль Верн в своем романе "20 тысяч лье под водой" предполагал создание машины, позволяющей человеку изучать морские глубины. Теперь батискафами, изобретенными Жаком Ивом Кусто, пользуется весь мир, совершенствуя знания о морской флоре и фауне. В 1990 году Гарри Гарриссон в романе "Спасательная шлюпка" описал создание сильных, здоровых, но генетически подавленных рабов. А теперь…
Может человечеству стоит задуматься над другими последствиями расшифровки генома человека, кроме искоренения наследственных заболеваний. Ведь не ровен час, когда они, эти последствия сами "свалятся нам на голову".
Вспоминая нацистские чистки, начитавшегося Ницше, Гитлера, испытания Водородной бомбы, попытки Генриха Гиммлера создать сверхчеловека, возникает вполне резонный вопрос: А ЧТО ДАЛЬШЕ?
Список литературы
1. Журнал "Техника Молодежи". Разные материалы за 1999-2000 г.;
2. Материалы, опубликованные в сети Интернет на сайтах www.kulichki.ru, www.lenta.ru, www.nature.com.